دوره 23، شماره 1 - ( فروردین و اردیبهشت 1399 )
جلد 23 شماره 1 صفحات 107-92 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Aliniya N, Elmieh A, Fadaei Chafy M. The Effect of Combined Training and Portulaca Oleracea Supplementation on Plasma Lipid Profile and Liver Ultrasound in Obese Females With Nonalcoholic Fatty Liver Disease. J Arak Uni Med Sci 2020; 23 (1) :92-107
URL: http://jams.arakmu.ac.ir/article-1-6132-fa.html
URL: http://jams.arakmu.ac.ir/article-1-6132-fa.html
علی نیا نرگس، علمیه علیرضا، فدائی چافی محمدرضا. اثر تمرین ترکیبی و مکمل خرفه بر غلظت پلاسمایی چربیهای خون و سونوگرافی کبد در زنان چاق مبتلا به کبد چرب غیرالکلی. مجله دانشگاه علوم پزشكي اراك. 1399; 23 (1) :92-107
1- گروه تربیت بدنی، دانشکده علوم انسانی، واحد رشت، دانشگاه آزاد اسلامی، رشت، ایران
2- گروه تربیت بدنی، دانشکده علوم انسانی، واحد رشت، دانشگاه آزاد اسلامی، رشت، ایران ،aliniya.n@yahoo.com
2- گروه تربیت بدنی، دانشکده علوم انسانی، واحد رشت، دانشگاه آزاد اسلامی، رشت، ایران ،
متن کامل [PDF 6314 kb]
(2454 دریافت)
| چکیده (HTML) (5080 مشاهده)
References
Sahebkar Khorasani MS, Azizi H, Yousefi M, Salari R, Bahrami-Taghanaki HR, Behravanrad P. [An evidence based review on integrative medicine in weight control (Persian)]. Complement Med J. 2017; 7(1):1828-50. http://cmja.arakmu.ac.ir/article-1-453-en.html
Safarpor M, Kohan L, Porkhajeh A. [Comparative study of anthropometric parameters in non-alcoholic fatty liver disease patients and healthy subjects (Persian)]. J Sabzevar Univ Med Sci. 2015; 22(3):225-31. http://jsums.medsab.ac.ir/article_555.html
Bahmanabadi Z, Ebrahimi-Mamghani M, Arefhosseini SR. [Comparision of low-calorie diet with and without sibutramine on body weight and liver function of patients with non-alcoholic fatty liver disease (Persian)]. Armaghan-e Danesh. 2011; 16(2):101-10. http://armaghanj.yums.ac.ir/article-1-378-en.html
Ghaemi AR, Taleban FA, Hekmatdoost A, Rafiei AR, Hosseini V, Amiri Z, et al. [Effect of weight reduction diet on non-alcoholic fatty liver disease (Persian)]. Iran J Nutr Sci Food Technol. 2013; 8(2):123-34. http://nsft.sbmu.ac.ir/article-1-1391-fa.html
Kaki A, Galedari M. [The effect of 12 weeks high intensity interval training and resistance training on liver fat, liver enzymes and insulin resistance in men with nonalcoholic fatty liver (Persian)]. Jundishapur Sci Med J. 2017; 16(5):493-503. [DOI:10.22118/JSMJ.2017.53990]
Davoodi M, Moosavi H, Nikbakht M. [The effect of eight weeks selected aerobic exercise on liver parenchyma and liver enzymes (AST, ALT) of fat liver patients (Persian)]. J Shahrekord Univ Med Sci. 2012; 14(1):84-90. http://journal.skums.ac.ir/article-1-1054-en.html
Nikroo H, Nematy M, Sima HR, Attarzade Hosseini SR, Pezeshki Rad M, Esmaeilzadeh A, et al. [Therapeutic effects of aerobic exercise and low-calorie diet on nonalcoholic steatohepatitis (Persian)]. Govaresh J. 2013; 17(4):245-51. http://govaresh.org/index.php/dd/article/view/1096
Shamsoddini A, Sobhani V, Ghamar Chehreh ME, Alavian SM, Zaree A. Effect of aerobic and resistance exercise training on liver enzymes and hepatic fat in Iranian men with nonalcoholic fatty liver disease. Hepat Mon. 2015; 15(10):e31434. [DOI:10.5812/hepatmon.31434] [PMID] [PMCID]
Changizi-Ashtiyani S, Zarei A, Taheri S, Rasekh F, Ramazani M. The effects of Portulaca oleracea alcoholic extract on induced hypercholesteroleomia in rats. Zahedan J Res Med Sci. 2012; 15(6):e92959. http://sites.kowsarpub.com/zjrms/articles/92959.html
Moosavi-Sohroforouzani A, Ganbarzadeh M. [Reviewing the physiological effects of aerobic and resistance training on insulin resistance and some biomarkers in non-alcoholic fatty liver disease (Persian)]. Feyz. 2016; 20(3):282-96. http://feyz.kaums.ac.ir/article-1-3091-en.html
Li J, Wang F, Chen K, Xia Y, Lu J, Zhou Y, et al. Effects of physical activity on liver function in patients with non-alcoholic fatty liver disease: A meta-analysis. SOJ Immunol. 2015; 3(5):1-6. [DOI:10.15226/2372-0948/3/5/00143]
Salehi A, Farzanegi P. [Effect of 8 weeks of resistance training with and without portulacalo seeds on some of liver injury markers in women with diabetes type 2 (Persian)]. Stud Med Sci. 2015; 25(11):968-78. http://umj.umsu.ac.ir/article-1-2603-en.html
El-Sayed MI. Effects of Portulaca oleracea L. seeds in treatment of type-2 diabetes mellitus patients as adjunctive and alternative therapy. J Ethnopharmacol. 2011; 137(1):643-51. [DOI:10.1016/j.jep.2011.06.020] [PMID]
Dehghan F, Soori R, Gholami K, Abolmaesoomi M, Yusof A, Muniandy S, et al. Purslane (Portulaca oleracea) seed consumption and aerobic training improves biomarkers associated with atherosclerosis in women with Type 2 Diabetes (T2D). Sci Rep. 2016; 6:37819. [DOI:10.1038/srep37819] [PMID] [PMCID]
Gheflati A, Adelnia E, Nadjarzadeh A. The clinical effects of purslane (Portulaca oleracea) seeds on metabolic profiles in patients with nonalcoholic fatty liver disease: A randomized controlled clinical trial. Phytother Res. 2019; 33(5):1501-9. [DOI:10.1002/ptr.6342] [PMID]
Esmaillzadeh A, Zakizadeh E, Faghihimani E, Gohari M, Jazayeri S. The effect of purslane seeds on glycemic status and lipid profiles of persons with type 2 diabetes: A randomized controlled cross-over clinical trial. J Res Med Sci. 2015; 20(1):47-53. [PMID] [PMCID]
Papoli M, Pishdad S, Nadjarzadeh A, Hosseinzadeh M. Effects of consuming purslane seed powder on indicators of metabolic syndrome in women: A randomized clinical trial. Prog Nutr. 2019; 21(Suppl. 1):329-35. [DOI:10.23751/pn.v21i1-S.6210]
Behzadimoghadam M, Galedari M, Motalebi L. [The effect of eight weeks resistance training and low-calorie diet on plasma levels of liver enzymes and liver fat in Non-Alcoholic Fatty Liver Disease (NAFLD) (Persian)]. Iran J Nutr Sci Food Technol. 2018; 12(4):25-32. http://nsft.sbmu.ac.ir/article-1-2356-en.html
متن کامل: (6299 مشاهده)
مقدمه
بر اساس گزارشهای سازمان بهداشت جهانی، اضافه وزن و چاقی پنجمین علت مرگومیر در جهان است. چاقی با بیماریهای مختلفی مانند دیابت نوع 2، سندروم متابولیک، بیماری کرونری قلب و بیماری اختلال چربی خون در ارتباط است. یکی از بیماریهای مهم که همبستگی قویتری با چاقی دارد، بیماری کبد چرب غیرالکلی است [1]. کبد چرب غیرالکلی، تجمع چربی بهویژه تری گلیسیرید در سیتوپلاسم سلولهای کبدی به میزان بیش از 5 الی10 درصد وزن کبد است و شایعترین بیماری کبدی در سرتاسر جهان به شمار میرود. شمار مبتلایان به این بیماری به دلیل تغییر شیوه زندگی، کاهش فعالیت بدنی و عادات تغذیهای نادرست در حال افزایش است [4-2]. روشهای مختلفی با اعتبارهای متفاوت برای تشخیص بیماری کبد چرب غیرالکلی توسعه یافتهاند.
این روشها شامل تصویربرداریهای مختلف، نمونهبرداری سوزنی، شاخصهای بیوشیمیایی و آنتروپومتریک است. متداولترین و قابلاجراترین روشهای ارزیابی برای تشخیص این بیماری، سنجش بالا بودن غلظت پلاسمایی چربیهای خون و آنزیمهای کبدی و نیز سونوگرافی از کبد است [5]. بالا بودن غلظت پلاسمایی چربیهای خون (کلسترول، تری گلیسرید، LDL) منجر به افزایش سنتز چربی در کبد و درنهایت تجمع چربی و ایجاد کبد چرب میشود [6] که از طریق بالارفتن مقدار غلظت سرمی چربیها قابل تشخیص است. تاکنون راهکار ثابت و مشخصی برای پیشگیری یا درمان بیماری کبد چرب بیان نشده است. درمان توصیهشده برای این بیماری شامل برنامههای کاهش وزن از طریق رژیم غذایی، فعالیت ورزشی منظم و عمل جراحی برای کاهش وزن در چاقیهای مفرط است [9-7].
مطالعات نشان دادهاند که فعالیت ورزشی هوازی به وسیله بهبود کنترل قند، اکسیداسیون چربی از طریق افزایش حملونقل گلوکز با انتقالدهنده گلوکز -4 در عضله مخطط، بیان و فعالیت آنزیم گلیکوژن سنتاز در گیرندههای انسولینی، ذخیره گلیکوژن در عضله و کبد، افزایش سنتز تری گلیسیرید در سلولهای عضلانی، کاهش انباشت متابولیتهای اسیدهای چرب و سرکوب حالت التهابی مرتبط با مقاومت انسولینی، این چرخه را نقض میکند [10].
تمرینات مقاومتی نیز موجب افزایش قدرت و توده عضلانی، کاهش چربی (چربی بدن، چربی احشایی و چربی زیرجلدی)، افزایش حساسیت انسولینی، افزایش پتانسیل مصرف اسیدهای چرب آزاد، افزایش متابولیسم پایه و متعاقب آن افزایش سوختن چربیهای بدن و درنتیجه کاهش وزن میشود [11]. تمرینات ترکیبی (هوازی و مقاومتی) نوع دیگری از تمرینات است که میتواند به مهار چربی کبد به وسیله افزایش انرژی مصرفی، بهتر کردن اکسیداسیون چربی، کاهش در چربی زیرپوستی و جریان اسید چرب آزاد به کبد کمک کند [12]. طب سنتی از گیاهان متنوعی برای درمان طیف وسیعی از بیماریها نظیر بیماریهای التهابی، دیابت و بسیاری از اختلالات کبدی و کلیوی استفاده کرده است؛ ازجمله این گیاهان خرفه است [9].
مطالعات نشان داده است که ترکیبات آنتیاکسیدانتی و اسیدهای چرب امگا - 3 و امگا - 6 موجود در عصاره خرفه از طریق افزایش مصرف انرژی و کاهش بیان آنزیمهای محدودکننده سرعت سنتز اسید چرب در کبد ( استیل کوآنزیم آ کربوکسیلاز و اسید چرب سنتتاز) باعث مهار پراکسیداسیون لیپید میشود. از سوی دیگر، خرفه حاوی مقادیر زیادی آلکالوئیدهای فنولیک است که این آلکالوئیدها نیز از طریق افزایش اسید چرب غیراشباع باعث مهار سنتز کلسترول میشوند [9]. در خصوص اثرات مقادیر مختلف دانه خرفه، ال-سید و همکاران [13] ، دهقانزاده و همکاران [14] و غفلتی و همکاران [15] کاهش معنیداری در سطح سرمی چربیهای خون (تری گلیسیرید، کلسترول تام، LDL) و افزایش قابلتوجه در سطح HDL هنگام مصرف دانه خرفه در بیماران دیابت نوع 2 را نشان دادهاند. اسماعیلزاده و همکاران [16] و پاپولی و همکاران ( 2019) [17] نشان دادهاند که مصرف دانه خرفه بر سطح چربیهای خون تأثیرگذار نیست.
با توجه به مطالعات انجامشده و نتایج بهدستآمده از پژوهشهای پیشین، اطلاعاتی متناقض در مورد اثر انواع تمرینات ورزشی در بیماران کبد چرب غیرالکلی وجود دارد؛ اما در مورد اثرات مکمل خرفه بر نشانههای بیوشیمیایی خون و وضعیت کبد در افراد مبتلا به کبد چرب و همچنین اثرات تعاملی تمرین و مکمل خرفه در این بیماران پژوهشهایی محدود صورت گرفته و اطلاعاتی کم در دست است. در بیشتر پژوهشهای انجامشده نیز از دانه خرفه استفاده شده است. با توجه به خواص درمانی قسمتهای مختلف گیاه خرفه (دانه، ساقه، برگ) که دارای ویژگیهای آنتیاکسیدانتی، آنتیدیابتی و کاهنده چربی خون است، همچنین بر اساس بررسیهای پژوهشگر به نظر میرسد تاکنون هیچ پژوهشی اثر تعاملی تمرینات ترکیبی و مکمل خرفه (ساقه و برگ) را در بیماران کبد چرب غیرالکلی بررسی نکرده است؛ بنابراین این مطالعه با هدف ترکیب تمرینات ترکیبی و مصرف مکمل خرفه به عنوان گیاه دارویی بیخطر [5] و یک آنتیاکسیدانی قوی در پیشگیری و کاهش استرس اکسیداتیو سلولهای کبدی، قصد دارد پاسخگوی ابهامات موجود در این زمینه باشد.
مواد و روشها
جامعه آماری پژوهش حاضر را زنان چاق 60-40 سال مبتلا به کبد چرب غیرالکلی استان گیلان (شهرستان آستارا) تشکیل دادند. آزمودنیها به روش غیرتصادفی از طریق فراخوان و اطلاعرسانی در مراکز سونوگرافی، آزمایشگاهها، داروخانهها و مراکز بهداشت انتخاب شدند. تعداد نمونههای مطالعه توسط نرمافزار جی پاور 40 نفر تخمین زده شد که به صورت نمونهگیری هدفمند انتخاب و در 4 گروه تمرین + مکمل (10 =n)، دارونما (10=n)، کنترل (10 =n) و مکمل (10=n) به صورت تصادفی و یکسویه کور قرار گرفتند. شرایط ورود به مطالعه شامل سن 60-40 سال، شاخص توده بدنی بالاتر از 30 کیلوگرم بر متر مربع، یائسه بودن، ابتلا به کبد چرب غیرالکلی دستکم درجه یک بود.
معیارهای خروج از پژوهش شامل ابتلا به بیماریهای قلبی–تنفسی، کلیوی، بیماریهای حاد (هپاتیت ویروسی B، C، هپاتیت خودایمنی، بیماری سلیاک، ویلسون، کمبود 1a آنتی ترییسین و هموکروماتوز، اختلالات مزمن یا حاد کبدی، سرطانها، انجام پیوند کبد)، بیماری هیپوتیروئیدی، بیماری فشار خون، اختلالات انعقادی، اختلال در سیستم ایمنی، استعمال دخانیات و مصرف الکل، استفاده از رژیم غذایی یا دارویی خاص، مصرف مکملها و گیاهان دارویی، انجام فعالیت منظم ورزشی ظرف 6 ماه گذشته، نداشتن منع شرکت در فعالیتهای ورزشی، هر گونه عمل جراحی و کاهش شدید وزن در 6 ماه گذشته بود [ 18، 7، 5].
این اطلاعات از طریق پرسشنامه سلامتی–پزشکی جمعآوری و به تأیید پزشک میرسید. اختصاص آزمودنیها به گروهها به صورت تصادفی ( قرعهکشی) بود. نحوه تقسیم تصادفی بر مبنای همگنسازی نتایج سونوگرافی بود، طوریکه هر کدام از 4 نفری که بالاترین میزان تجمع چربی کبد را داشتند، به قید قرعه در یکی از 4 گروه فوق قرار گرفتند و در مورد 4 نفر بعدی و نفرات آخر نیز بدینگونه عمل شد. بعد از انتخاب نمونهها، جلسه توجیهی با افراد واجد شرایط گذاشته و اطلاعات لازم به آنها در مورد اهداف پژوهش، روش انجام کار، فعالیتهای درنظرگرفتهشده در طول پژوهش، استفاده از مکمل گیاهی، دفعات خونگیری و قوانین و مقرارات ورود و خروج از مطالعه و انصراف در صورت عدم رضایت داده شد و افراد شرکتکننده در مطالعه، فرم رضایت کتبی آگاهانه در تحقیق را تکمیل کردند.
قبل و 24 ساعت بعد از آخرین جلسه تمرینی، شاخصهای آنتروپومتریکی و فیزیولوژیکی آزمودنیها (قد، وزن، دور کمر، دور باسن، درصد چربی، قدرت عضلانی، توان هوازی، پارانشیم کبدی) اندازهگیری شد. برنامه تمرین شامل برنامه تمرین ترکیبی (هوازی و مقاومتی) به مدت 90 دقیقه در روز و از ساعت 30/5-4 بعدازظهر بود؛ به این ترتیب که در یک روز و در نیمه ابتدای یک جلسه، تمرینات هوازی و در نیمه دوم آن تمرینات قدرتی انجام شد. برنامه تمرین هوازی شامل انواع حرکات ایروبیک از ساده به ترکیبی به مدت 12 هفته، 3 جلسه در هفته و هر جلسه 65-45 دقیقه با شدت 60 الی80 درصد ضربان قلب بیشینه بود که با افزایش تدریجی شدت و مدت تمرین در هر هفته همراه بود. شدت تمرین بر اساس نسبتی از ضربان قلب بیشینه محاسبه و همچنین ضربان قلب به وسیله ضربانسنج پولار کنترل شد. برنامه تمرین هوازی در هر جلسه شامل گرم کردن (10 دقیقه)، حرکات ایروبیک (55-25 دقیقه)، سرد کردن (10 دقیقه) بود [18].
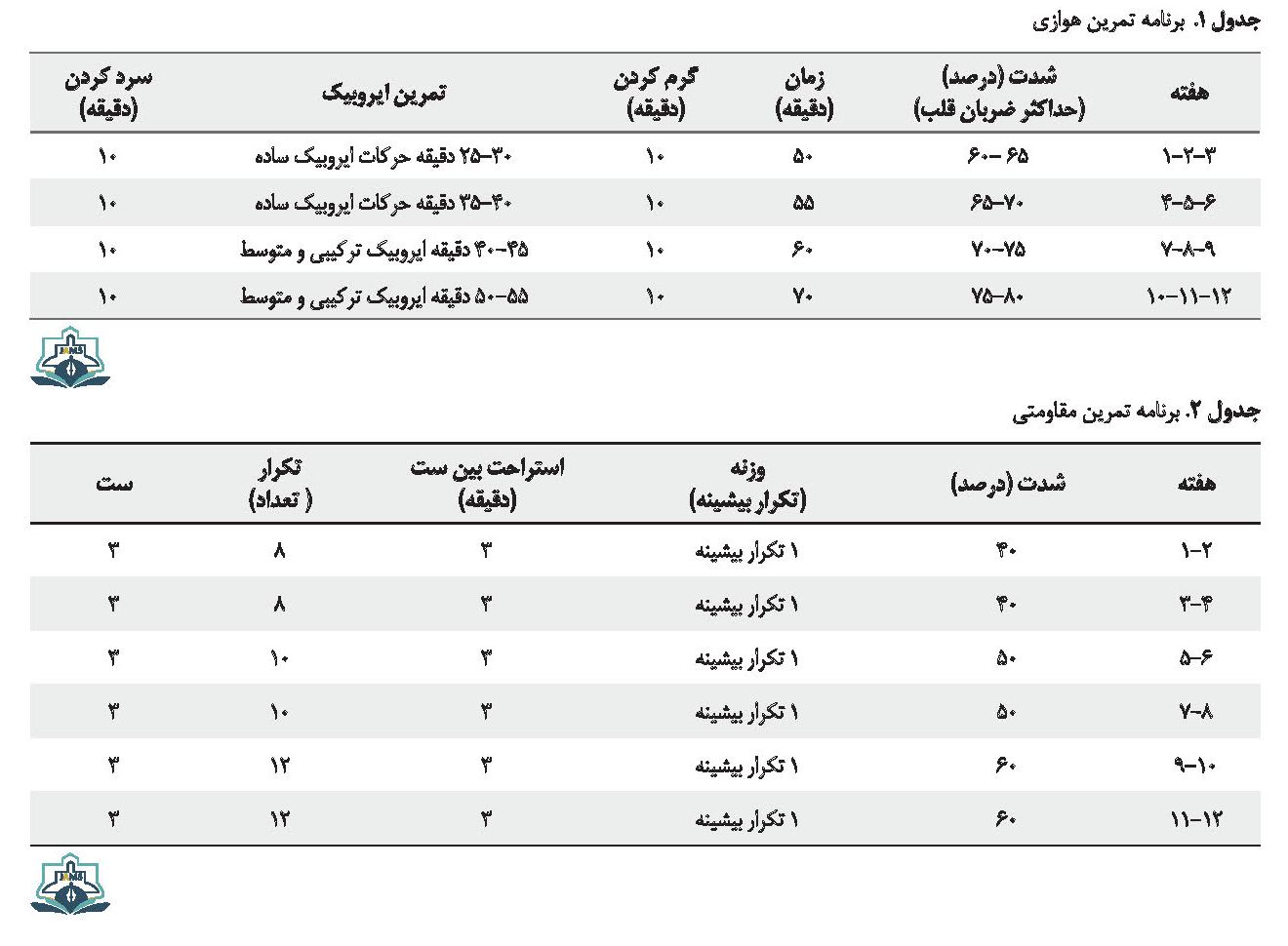
حرکات ایروبیک به 3 دسته حرکات ایروبیک ساده، متوسط و ترکیبی تقسیم شد. حرکات ایروبیک ساده و متوسط شامل انجام تک حرکت به صورت مجزا برای اندامهای فوقانی، تحتانی و تنه و نیز انواع حرکات همراه با جابهجایی میشد که میتوان به حرکت مارچ، حرکت وی، وی بک، مورب و حرکات برگشت به سمت عقب اشاره کرد. حرکات ایروبیک ترکیبی شامل ترکیبی ازحرکات ایروبیک ساده و متوسط با استفاده از ابزارهای مختلف موجود مانند استپ، چوب و کش بود. برنامه تمرین مقاومتی به مدت 12 هفته، 3 جلسه در هفته و هر جلسه با شدت 60 -40 درصد یک تکرار بیشینه، 3 ست با 8 تا 12 تکرار و فواصل استراحتی بین هر ست 3 دقیقه بود. 8 حرکت تمرین مقاومتی شامل حرکت جلو بازو با دمبل، پرس سینه با دمبل، حرکت کشش دست به پایین با دستگاه، حرکت قایقی با دستگاه قایقی، جلو ران با دستگاه، پشت ران خوابیده با دستگاه، پرس پا با دستگاه و دراز و نشست با دستگاه بود [6] (جدول شماره 1).
در جدول شماره 2 برنامه تمرین مقاومتی نشان داده شده است. در این پژوهش از کپسول خرفه ( پرپین آلا) استفاده شد که بر اساس اطلاعات موجود در بروشور آن، در ساخت این کپسول از قسمتهای هوایی گیاه خرفه شامل برگ، ساقه و دانههای آن استفاده شده است. در جدول شماره 3 ترکیبات کپسول خرفه نشان داده شده است. گروه مکمل + تمرین و گروه مکمل، روزانه 2 کپسول 500 میلیگرمی خرفه دریافت کردند. گروه دارونما نیز روزانه 2 کپسول دارونما (قرص حاوی آرد گندم) دریافت کردند.
برای اطمینان از مصرف وعدهها، کپسولها به صورت هفتگی توزیع و همراه با توصیههای لازم (برای میزان و زمان مصرف) در اختیار شرکتکنندگان قرار گرفت. به افراد هر دو گروه آموزش داده شد که باید هر روز کپسول را در دو نوبت بعد از وعده صبحانه و شام مصرف کنند. برای اجرای این کار، کپسولهای مربوط در بستهبندیهای مشابه با اطلاعات و دستورالعمل یکسان بستهبندی و توسط فردی غیر از مداخلهگر به صورت A، B کدگذاری شد تا عدم اطلاع مداخلهگر از نوع کپسول دریافتی توسط هر گروه رعایت شود. برای پیگیری مصرف مکمل توسط افراد مورد مطالعه، روزانه با این افراد تماس گرفته شد و مقادیر مصرفی ادعاشده پیگیری و اطلاعات لازم دریافت شد و آزمودنیهایی که قرصهای خود را مصرف نکرده بودند، از مطالعه کنار گذاشته شدند. در جدول شماره 4 نحوه مصرف مکمل– دارونما درگروهها نشان داده شده است.
رژیم غذایی آزمودنیها تحت نظر یک متخصص تغذیه از طریق فرم یادآمد خوراکی یک هفته قبل از شروع برنامه تمرینی تا پایان مطالعه کنترل شد. یک هفته قبل از شروع تمرین و 72 ساعت بعد از آخرین جلسه تمرین، خونگیری (مقدار 5 میلیلیتر خون) انجام شد. سطح چربیهای خون با استفاده از کیتهای شرکت پارسآزمون (ساخت ایران، کرج) و با روش رنگسنجی آنزیماتیک تعیین شد. در پژوهش حاضر به دلیل سن بالای آزمودنیها و عدم امکان ترمیم کامل سلولهای کبدی و همچنین عدم ابتلای بیماران به بیماری مزمن کبدی (سیروز کبدی) انجام بیوپسی کبد امکانپذیر نبود. با بررسی پژوهشهای مشابه انجامشده در خصوص اندازهگیری تجمع چربی کبد و نیز با توجه به اینکه در بین روشهای اندازهگیری، قابلاجراترین و در دسترسترین روش سونوگرافی (با حساسیت اندازهگیری 3/73 تا 5/90 درصد) بود؛ لذا برای اندازهگیری شدت تجمع چربی کبد از این روش استفاده شد [18].
سونوگرافی را متخصص تصویربرداری پزشکی با استفاده از دستگاه سونوگرافی کالرداپلر ESAOTE مدل 40 MY LAB ساخت کشور ایتالیا انجام داد. سونوگرافی از ناحیه شکم آزمودنیها انجام و به صورت کیفی یعنی مشخص کردن درجه تجمع چربی کبد (1، 2 یا 3) گزارش شد. کبد روشن در سونوگرافی نشانه رسوب چربی در کبد است. با افزایش تجمع چربی در کبد، حاشیه عروق محو میشود و در موارد شدیدتر، نفوذ صوت به اعماق کبد کاهش مییابد و قسمتهای خلفی لوب راست خوب دیده نمیشوند. شدت تجمع چربی در کبد به صورت درجه صفر (بدون تجمع چربی)، درجه 1 (کبد چرب خفیف)، درجه 2 ( متوسط) و درجه 3 ( شدید) درجهبندی شد. از آزمودنیها دعوت شد تا در روز مقرر به مرکز سونوگرافی مراجعه کنند و به منظور مشخص کردن هر چه دقیقتر میزان چربی کبد (درجه 1، درجه 2، درجه 3)، حداقل 4 تا 6 ساعت ناشتا باشند. یک متخصص رادیولوژیست با دستگاه سونوگرافی کالرداپلر ESAOTE مدل 40 MY LAB ساخت کشور ایتالیا از کبد تمامی افراد سونوگرافی نجام داد. 48 ساعت بعد از آخرین جلسه تمرین مجدداً سونوگرافی انجام شد [5].
به استثنای دادههای مربوط به سونوگرافی کبد که دارای مقیاس اسمی بودند و به صورت نما گزارش شدند، کلیه مقادیر به صورت میانگین به اضافه یا منهای انحراف استاندارد ارائه شدند. برای تجزیهوتحلیل دادهها از SPSS نسخه 25 استفاده و سطح معناداری، کوچکتر و مساوی با 05/0 در نظر گرفته شد. برای سنجیدن طبیعی بودن توزیع دادهها از آزمون شاپیرو- ویلک، برای بررسی تغییرات درونگروهی از آزمون تی همبسته، برای بررسی تغییرات بین گروهها از آزمون تحلیل واریانس یکطرفه و پس از برقراری پیشفرض نرمال بودن توزیع دادهها و همگنی واریانسها ( آزمون لون) از آزمون تعقیبی توکی در صورت معنیدار بودن نتایج آزمون تحلیل واریانس و برای ترسیم نمودارها از نرمافزار EXCEL نسخه 2013 استفاده شد.
یافتهها
نتایج حاصل از بررسی نرمال بودن دادهها به کمک آزمون شاپیروویک نشان داد که دادهها در متغییرهای مورد نظر دارای توزیع طبیعی هستند (05/P<0). ویژگیهای آنتروپومتریک آزمودنیها در جدول شماره 5 نشان داده شده است.
بر اساس گزارشهای سازمان بهداشت جهانی، اضافه وزن و چاقی پنجمین علت مرگومیر در جهان است. چاقی با بیماریهای مختلفی مانند دیابت نوع 2، سندروم متابولیک، بیماری کرونری قلب و بیماری اختلال چربی خون در ارتباط است. یکی از بیماریهای مهم که همبستگی قویتری با چاقی دارد، بیماری کبد چرب غیرالکلی است [1]. کبد چرب غیرالکلی، تجمع چربی بهویژه تری گلیسیرید در سیتوپلاسم سلولهای کبدی به میزان بیش از 5 الی10 درصد وزن کبد است و شایعترین بیماری کبدی در سرتاسر جهان به شمار میرود. شمار مبتلایان به این بیماری به دلیل تغییر شیوه زندگی، کاهش فعالیت بدنی و عادات تغذیهای نادرست در حال افزایش است [4-2]. روشهای مختلفی با اعتبارهای متفاوت برای تشخیص بیماری کبد چرب غیرالکلی توسعه یافتهاند.
این روشها شامل تصویربرداریهای مختلف، نمونهبرداری سوزنی، شاخصهای بیوشیمیایی و آنتروپومتریک است. متداولترین و قابلاجراترین روشهای ارزیابی برای تشخیص این بیماری، سنجش بالا بودن غلظت پلاسمایی چربیهای خون و آنزیمهای کبدی و نیز سونوگرافی از کبد است [5]. بالا بودن غلظت پلاسمایی چربیهای خون (کلسترول، تری گلیسرید، LDL) منجر به افزایش سنتز چربی در کبد و درنهایت تجمع چربی و ایجاد کبد چرب میشود [6] که از طریق بالارفتن مقدار غلظت سرمی چربیها قابل تشخیص است. تاکنون راهکار ثابت و مشخصی برای پیشگیری یا درمان بیماری کبد چرب بیان نشده است. درمان توصیهشده برای این بیماری شامل برنامههای کاهش وزن از طریق رژیم غذایی، فعالیت ورزشی منظم و عمل جراحی برای کاهش وزن در چاقیهای مفرط است [9-7].
مطالعات نشان دادهاند که فعالیت ورزشی هوازی به وسیله بهبود کنترل قند، اکسیداسیون چربی از طریق افزایش حملونقل گلوکز با انتقالدهنده گلوکز -4 در عضله مخطط، بیان و فعالیت آنزیم گلیکوژن سنتاز در گیرندههای انسولینی، ذخیره گلیکوژن در عضله و کبد، افزایش سنتز تری گلیسیرید در سلولهای عضلانی، کاهش انباشت متابولیتهای اسیدهای چرب و سرکوب حالت التهابی مرتبط با مقاومت انسولینی، این چرخه را نقض میکند [10].
تمرینات مقاومتی نیز موجب افزایش قدرت و توده عضلانی، کاهش چربی (چربی بدن، چربی احشایی و چربی زیرجلدی)، افزایش حساسیت انسولینی، افزایش پتانسیل مصرف اسیدهای چرب آزاد، افزایش متابولیسم پایه و متعاقب آن افزایش سوختن چربیهای بدن و درنتیجه کاهش وزن میشود [11]. تمرینات ترکیبی (هوازی و مقاومتی) نوع دیگری از تمرینات است که میتواند به مهار چربی کبد به وسیله افزایش انرژی مصرفی، بهتر کردن اکسیداسیون چربی، کاهش در چربی زیرپوستی و جریان اسید چرب آزاد به کبد کمک کند [12]. طب سنتی از گیاهان متنوعی برای درمان طیف وسیعی از بیماریها نظیر بیماریهای التهابی، دیابت و بسیاری از اختلالات کبدی و کلیوی استفاده کرده است؛ ازجمله این گیاهان خرفه است [9].
مطالعات نشان داده است که ترکیبات آنتیاکسیدانتی و اسیدهای چرب امگا - 3 و امگا - 6 موجود در عصاره خرفه از طریق افزایش مصرف انرژی و کاهش بیان آنزیمهای محدودکننده سرعت سنتز اسید چرب در کبد ( استیل کوآنزیم آ کربوکسیلاز و اسید چرب سنتتاز) باعث مهار پراکسیداسیون لیپید میشود. از سوی دیگر، خرفه حاوی مقادیر زیادی آلکالوئیدهای فنولیک است که این آلکالوئیدها نیز از طریق افزایش اسید چرب غیراشباع باعث مهار سنتز کلسترول میشوند [9]. در خصوص اثرات مقادیر مختلف دانه خرفه، ال-سید و همکاران [13] ، دهقانزاده و همکاران [14] و غفلتی و همکاران [15] کاهش معنیداری در سطح سرمی چربیهای خون (تری گلیسیرید، کلسترول تام، LDL) و افزایش قابلتوجه در سطح HDL هنگام مصرف دانه خرفه در بیماران دیابت نوع 2 را نشان دادهاند. اسماعیلزاده و همکاران [16] و پاپولی و همکاران ( 2019) [17] نشان دادهاند که مصرف دانه خرفه بر سطح چربیهای خون تأثیرگذار نیست.
با توجه به مطالعات انجامشده و نتایج بهدستآمده از پژوهشهای پیشین، اطلاعاتی متناقض در مورد اثر انواع تمرینات ورزشی در بیماران کبد چرب غیرالکلی وجود دارد؛ اما در مورد اثرات مکمل خرفه بر نشانههای بیوشیمیایی خون و وضعیت کبد در افراد مبتلا به کبد چرب و همچنین اثرات تعاملی تمرین و مکمل خرفه در این بیماران پژوهشهایی محدود صورت گرفته و اطلاعاتی کم در دست است. در بیشتر پژوهشهای انجامشده نیز از دانه خرفه استفاده شده است. با توجه به خواص درمانی قسمتهای مختلف گیاه خرفه (دانه، ساقه، برگ) که دارای ویژگیهای آنتیاکسیدانتی، آنتیدیابتی و کاهنده چربی خون است، همچنین بر اساس بررسیهای پژوهشگر به نظر میرسد تاکنون هیچ پژوهشی اثر تعاملی تمرینات ترکیبی و مکمل خرفه (ساقه و برگ) را در بیماران کبد چرب غیرالکلی بررسی نکرده است؛ بنابراین این مطالعه با هدف ترکیب تمرینات ترکیبی و مصرف مکمل خرفه به عنوان گیاه دارویی بیخطر [5] و یک آنتیاکسیدانی قوی در پیشگیری و کاهش استرس اکسیداتیو سلولهای کبدی، قصد دارد پاسخگوی ابهامات موجود در این زمینه باشد.
مواد و روشها
جامعه آماری پژوهش حاضر را زنان چاق 60-40 سال مبتلا به کبد چرب غیرالکلی استان گیلان (شهرستان آستارا) تشکیل دادند. آزمودنیها به روش غیرتصادفی از طریق فراخوان و اطلاعرسانی در مراکز سونوگرافی، آزمایشگاهها، داروخانهها و مراکز بهداشت انتخاب شدند. تعداد نمونههای مطالعه توسط نرمافزار جی پاور 40 نفر تخمین زده شد که به صورت نمونهگیری هدفمند انتخاب و در 4 گروه تمرین + مکمل (10 =n)، دارونما (10=n)، کنترل (10 =n) و مکمل (10=n) به صورت تصادفی و یکسویه کور قرار گرفتند. شرایط ورود به مطالعه شامل سن 60-40 سال، شاخص توده بدنی بالاتر از 30 کیلوگرم بر متر مربع، یائسه بودن، ابتلا به کبد چرب غیرالکلی دستکم درجه یک بود.
معیارهای خروج از پژوهش شامل ابتلا به بیماریهای قلبی–تنفسی، کلیوی، بیماریهای حاد (هپاتیت ویروسی B، C، هپاتیت خودایمنی، بیماری سلیاک، ویلسون، کمبود 1a آنتی ترییسین و هموکروماتوز، اختلالات مزمن یا حاد کبدی، سرطانها، انجام پیوند کبد)، بیماری هیپوتیروئیدی، بیماری فشار خون، اختلالات انعقادی، اختلال در سیستم ایمنی، استعمال دخانیات و مصرف الکل، استفاده از رژیم غذایی یا دارویی خاص، مصرف مکملها و گیاهان دارویی، انجام فعالیت منظم ورزشی ظرف 6 ماه گذشته، نداشتن منع شرکت در فعالیتهای ورزشی، هر گونه عمل جراحی و کاهش شدید وزن در 6 ماه گذشته بود [ 18، 7، 5].
این اطلاعات از طریق پرسشنامه سلامتی–پزشکی جمعآوری و به تأیید پزشک میرسید. اختصاص آزمودنیها به گروهها به صورت تصادفی ( قرعهکشی) بود. نحوه تقسیم تصادفی بر مبنای همگنسازی نتایج سونوگرافی بود، طوریکه هر کدام از 4 نفری که بالاترین میزان تجمع چربی کبد را داشتند، به قید قرعه در یکی از 4 گروه فوق قرار گرفتند و در مورد 4 نفر بعدی و نفرات آخر نیز بدینگونه عمل شد. بعد از انتخاب نمونهها، جلسه توجیهی با افراد واجد شرایط گذاشته و اطلاعات لازم به آنها در مورد اهداف پژوهش، روش انجام کار، فعالیتهای درنظرگرفتهشده در طول پژوهش، استفاده از مکمل گیاهی، دفعات خونگیری و قوانین و مقرارات ورود و خروج از مطالعه و انصراف در صورت عدم رضایت داده شد و افراد شرکتکننده در مطالعه، فرم رضایت کتبی آگاهانه در تحقیق را تکمیل کردند.
قبل و 24 ساعت بعد از آخرین جلسه تمرینی، شاخصهای آنتروپومتریکی و فیزیولوژیکی آزمودنیها (قد، وزن، دور کمر، دور باسن، درصد چربی، قدرت عضلانی، توان هوازی، پارانشیم کبدی) اندازهگیری شد. برنامه تمرین شامل برنامه تمرین ترکیبی (هوازی و مقاومتی) به مدت 90 دقیقه در روز و از ساعت 30/5-4 بعدازظهر بود؛ به این ترتیب که در یک روز و در نیمه ابتدای یک جلسه، تمرینات هوازی و در نیمه دوم آن تمرینات قدرتی انجام شد. برنامه تمرین هوازی شامل انواع حرکات ایروبیک از ساده به ترکیبی به مدت 12 هفته، 3 جلسه در هفته و هر جلسه 65-45 دقیقه با شدت 60 الی80 درصد ضربان قلب بیشینه بود که با افزایش تدریجی شدت و مدت تمرین در هر هفته همراه بود. شدت تمرین بر اساس نسبتی از ضربان قلب بیشینه محاسبه و همچنین ضربان قلب به وسیله ضربانسنج پولار کنترل شد. برنامه تمرین هوازی در هر جلسه شامل گرم کردن (10 دقیقه)، حرکات ایروبیک (55-25 دقیقه)، سرد کردن (10 دقیقه) بود [18].
حرکات ایروبیک به 3 دسته حرکات ایروبیک ساده، متوسط و ترکیبی تقسیم شد. حرکات ایروبیک ساده و متوسط شامل انجام تک حرکت به صورت مجزا برای اندامهای فوقانی، تحتانی و تنه و نیز انواع حرکات همراه با جابهجایی میشد که میتوان به حرکت مارچ، حرکت وی، وی بک، مورب و حرکات برگشت به سمت عقب اشاره کرد. حرکات ایروبیک ترکیبی شامل ترکیبی ازحرکات ایروبیک ساده و متوسط با استفاده از ابزارهای مختلف موجود مانند استپ، چوب و کش بود. برنامه تمرین مقاومتی به مدت 12 هفته، 3 جلسه در هفته و هر جلسه با شدت 60 -40 درصد یک تکرار بیشینه، 3 ست با 8 تا 12 تکرار و فواصل استراحتی بین هر ست 3 دقیقه بود. 8 حرکت تمرین مقاومتی شامل حرکت جلو بازو با دمبل، پرس سینه با دمبل، حرکت کشش دست به پایین با دستگاه، حرکت قایقی با دستگاه قایقی، جلو ران با دستگاه، پشت ران خوابیده با دستگاه، پرس پا با دستگاه و دراز و نشست با دستگاه بود [6] (جدول شماره 1).
در جدول شماره 2 برنامه تمرین مقاومتی نشان داده شده است. در این پژوهش از کپسول خرفه ( پرپین آلا) استفاده شد که بر اساس اطلاعات موجود در بروشور آن، در ساخت این کپسول از قسمتهای هوایی گیاه خرفه شامل برگ، ساقه و دانههای آن استفاده شده است. در جدول شماره 3 ترکیبات کپسول خرفه نشان داده شده است. گروه مکمل + تمرین و گروه مکمل، روزانه 2 کپسول 500 میلیگرمی خرفه دریافت کردند. گروه دارونما نیز روزانه 2 کپسول دارونما (قرص حاوی آرد گندم) دریافت کردند.
برای اطمینان از مصرف وعدهها، کپسولها به صورت هفتگی توزیع و همراه با توصیههای لازم (برای میزان و زمان مصرف) در اختیار شرکتکنندگان قرار گرفت. به افراد هر دو گروه آموزش داده شد که باید هر روز کپسول را در دو نوبت بعد از وعده صبحانه و شام مصرف کنند. برای اجرای این کار، کپسولهای مربوط در بستهبندیهای مشابه با اطلاعات و دستورالعمل یکسان بستهبندی و توسط فردی غیر از مداخلهگر به صورت A، B کدگذاری شد تا عدم اطلاع مداخلهگر از نوع کپسول دریافتی توسط هر گروه رعایت شود. برای پیگیری مصرف مکمل توسط افراد مورد مطالعه، روزانه با این افراد تماس گرفته شد و مقادیر مصرفی ادعاشده پیگیری و اطلاعات لازم دریافت شد و آزمودنیهایی که قرصهای خود را مصرف نکرده بودند، از مطالعه کنار گذاشته شدند. در جدول شماره 4 نحوه مصرف مکمل– دارونما درگروهها نشان داده شده است.
رژیم غذایی آزمودنیها تحت نظر یک متخصص تغذیه از طریق فرم یادآمد خوراکی یک هفته قبل از شروع برنامه تمرینی تا پایان مطالعه کنترل شد. یک هفته قبل از شروع تمرین و 72 ساعت بعد از آخرین جلسه تمرین، خونگیری (مقدار 5 میلیلیتر خون) انجام شد. سطح چربیهای خون با استفاده از کیتهای شرکت پارسآزمون (ساخت ایران، کرج) و با روش رنگسنجی آنزیماتیک تعیین شد. در پژوهش حاضر به دلیل سن بالای آزمودنیها و عدم امکان ترمیم کامل سلولهای کبدی و همچنین عدم ابتلای بیماران به بیماری مزمن کبدی (سیروز کبدی) انجام بیوپسی کبد امکانپذیر نبود. با بررسی پژوهشهای مشابه انجامشده در خصوص اندازهگیری تجمع چربی کبد و نیز با توجه به اینکه در بین روشهای اندازهگیری، قابلاجراترین و در دسترسترین روش سونوگرافی (با حساسیت اندازهگیری 3/73 تا 5/90 درصد) بود؛ لذا برای اندازهگیری شدت تجمع چربی کبد از این روش استفاده شد [18].
سونوگرافی را متخصص تصویربرداری پزشکی با استفاده از دستگاه سونوگرافی کالرداپلر ESAOTE مدل 40 MY LAB ساخت کشور ایتالیا انجام داد. سونوگرافی از ناحیه شکم آزمودنیها انجام و به صورت کیفی یعنی مشخص کردن درجه تجمع چربی کبد (1، 2 یا 3) گزارش شد. کبد روشن در سونوگرافی نشانه رسوب چربی در کبد است. با افزایش تجمع چربی در کبد، حاشیه عروق محو میشود و در موارد شدیدتر، نفوذ صوت به اعماق کبد کاهش مییابد و قسمتهای خلفی لوب راست خوب دیده نمیشوند. شدت تجمع چربی در کبد به صورت درجه صفر (بدون تجمع چربی)، درجه 1 (کبد چرب خفیف)، درجه 2 ( متوسط) و درجه 3 ( شدید) درجهبندی شد. از آزمودنیها دعوت شد تا در روز مقرر به مرکز سونوگرافی مراجعه کنند و به منظور مشخص کردن هر چه دقیقتر میزان چربی کبد (درجه 1، درجه 2، درجه 3)، حداقل 4 تا 6 ساعت ناشتا باشند. یک متخصص رادیولوژیست با دستگاه سونوگرافی کالرداپلر ESAOTE مدل 40 MY LAB ساخت کشور ایتالیا از کبد تمامی افراد سونوگرافی نجام داد. 48 ساعت بعد از آخرین جلسه تمرین مجدداً سونوگرافی انجام شد [5].
به استثنای دادههای مربوط به سونوگرافی کبد که دارای مقیاس اسمی بودند و به صورت نما گزارش شدند، کلیه مقادیر به صورت میانگین به اضافه یا منهای انحراف استاندارد ارائه شدند. برای تجزیهوتحلیل دادهها از SPSS نسخه 25 استفاده و سطح معناداری، کوچکتر و مساوی با 05/0 در نظر گرفته شد. برای سنجیدن طبیعی بودن توزیع دادهها از آزمون شاپیرو- ویلک، برای بررسی تغییرات درونگروهی از آزمون تی همبسته، برای بررسی تغییرات بین گروهها از آزمون تحلیل واریانس یکطرفه و پس از برقراری پیشفرض نرمال بودن توزیع دادهها و همگنی واریانسها ( آزمون لون) از آزمون تعقیبی توکی در صورت معنیدار بودن نتایج آزمون تحلیل واریانس و برای ترسیم نمودارها از نرمافزار EXCEL نسخه 2013 استفاده شد.
یافتهها
نتایج حاصل از بررسی نرمال بودن دادهها به کمک آزمون شاپیروویک نشان داد که دادهها در متغییرهای مورد نظر دارای توزیع طبیعی هستند (05/P<0). ویژگیهای آنتروپومتریک آزمودنیها در جدول شماره 5 نشان داده شده است.
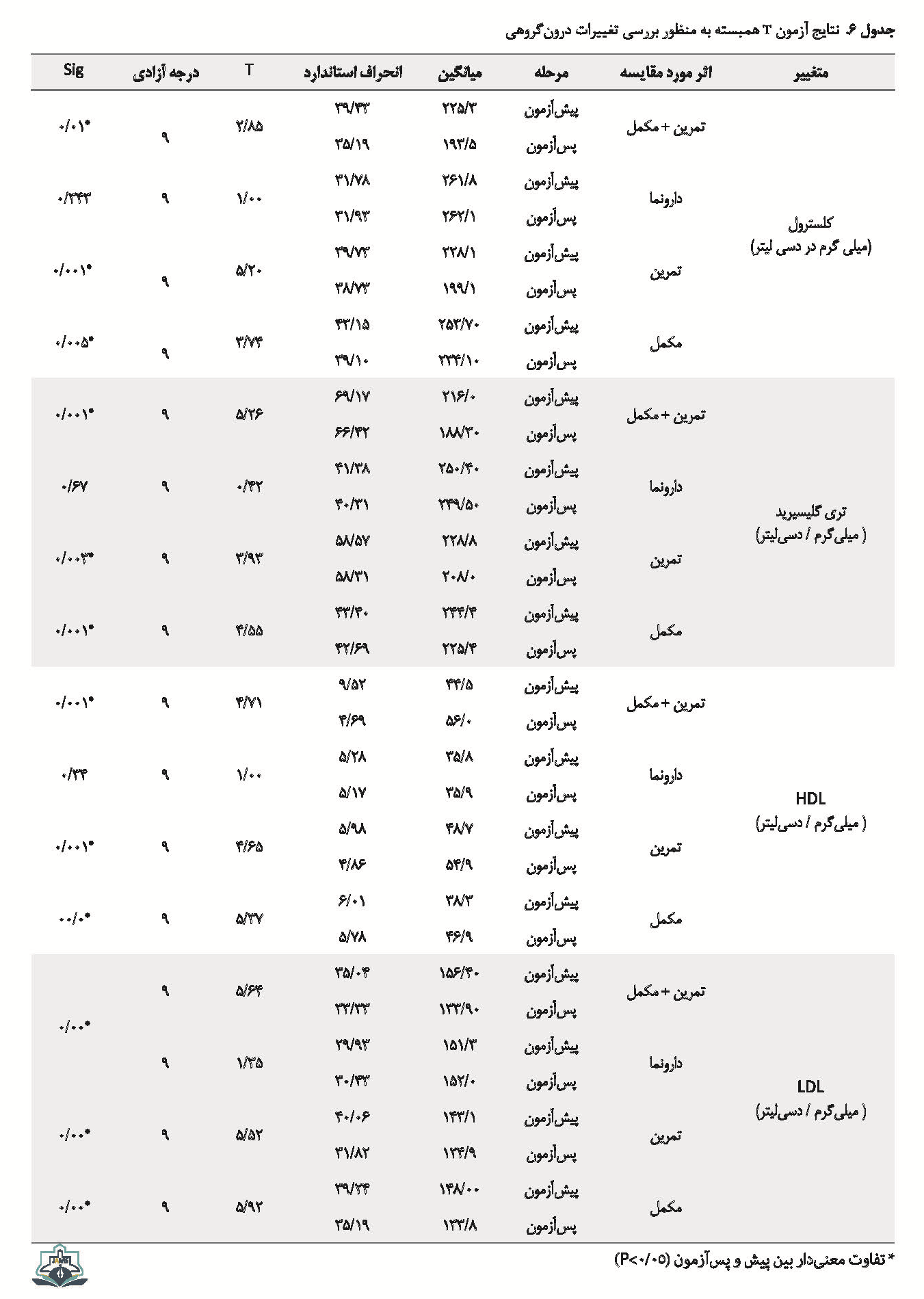
از آزمون پارامتریک تی همبسته (بررسی تفاوت درونگروهی) نیز استفاده شد. نتایج حاصل از آزمون تی همبسته نشان داد که پس از 12 هفته تمرین هوازی و مقاومتی، سطح سرمی کلسترول، LDL و تری گلیسیرید در گروه تمرین + مکمل، گروه تمرین و گروه مکمل کاهش معنیداری داشته است ( 0/05>P)، اما سطح سرمی HDL افزایش معنیداری را نشان داد ( 0/05> P). در جدول شماره 6 نتایج به تفصیل نشان داده شده است.
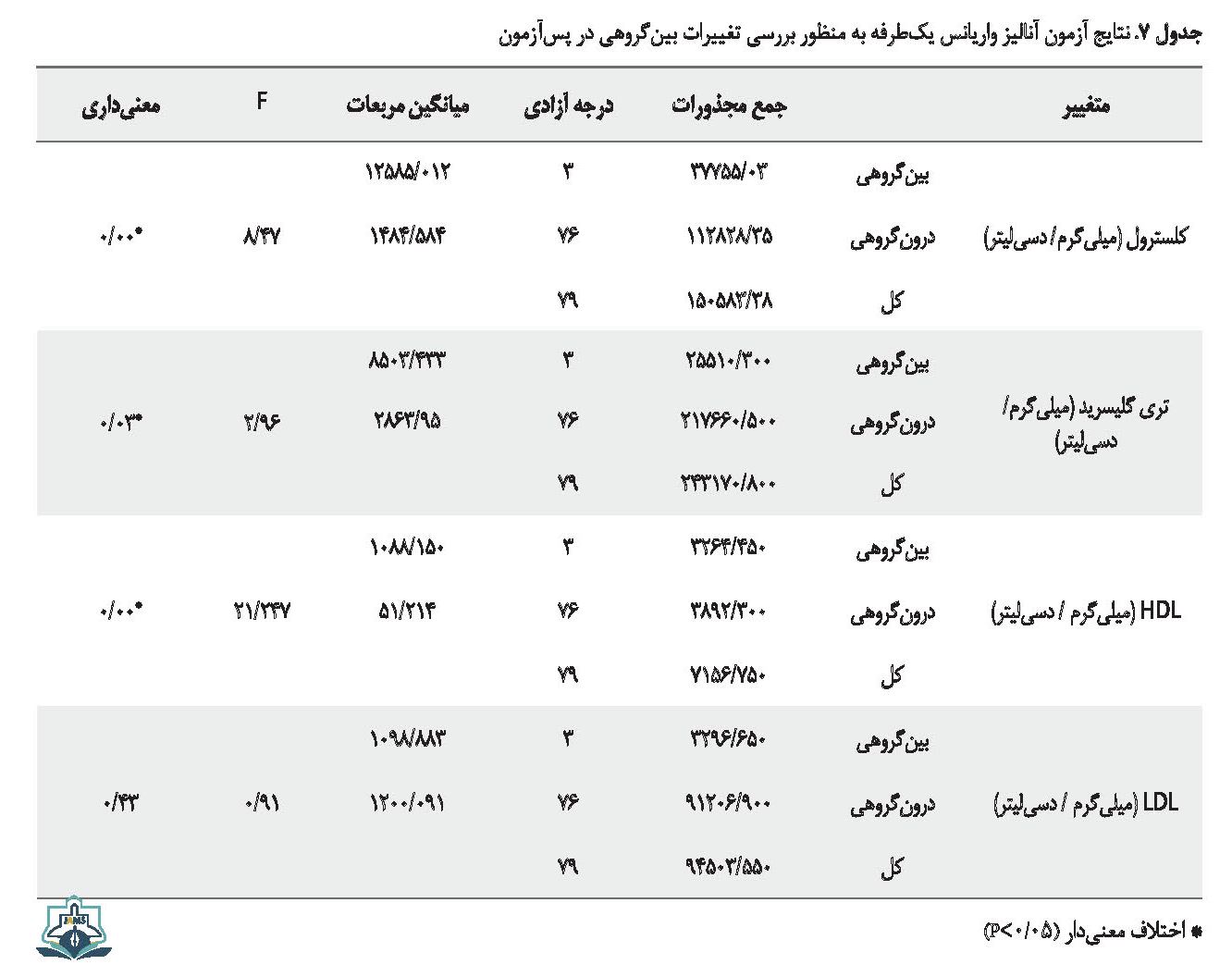
نتایج حاصل از آزمون لون هم نشان داد که دادهها معنیدار هستند، بنابراین از آزمون تحلیل واریانس یکطرفه برای بررسی تفاوتهای بینگروهی استفاده شد. آزمون تحلیل آنووا یکطرفه نیز نشان داد که تفاوت معنیداری در مقایسه بین گروهها موجود دارد ( 0/05>P) که نتایج در جدول شماره 7 نشان داده شده است. با توجه به مشاهده تفاوتهای بینگروهی در نتیجه آزمون آنووای یکراهه، برای بررسی دقیقتر و مقایسه دو به دوی آزمونها از آزمون تعقیبی توکی استفاده شد.
نتایج آزمون تعقیبی توکی مشخص کرد که در میزان تغییرات کلسترول، تفاوت معنیداری بین گروههای تمرین + مکمل با گروه دارونما، گروه دارونما با گروه تمرین وجود دارد. در میزان تغییرات تری گلیسیرید، تفاوت معنیداری بین گروههای تمرین + مکمل با گروه دارونما وجود دارد. در میزان تغییرات آنزیم HDL، تفاوت معنیداری بین گروه تمرین + مکمل با گروه دارونما، گروه تمرین + مکمل با گروه مکمل، همچنین بین گروه دارونما با گرو تمرین و نیز بین گروه تمرین با گروه مکمل وجود دارد (0/05>P). نتایج در جدول شماره 8 نشان داده شده است.
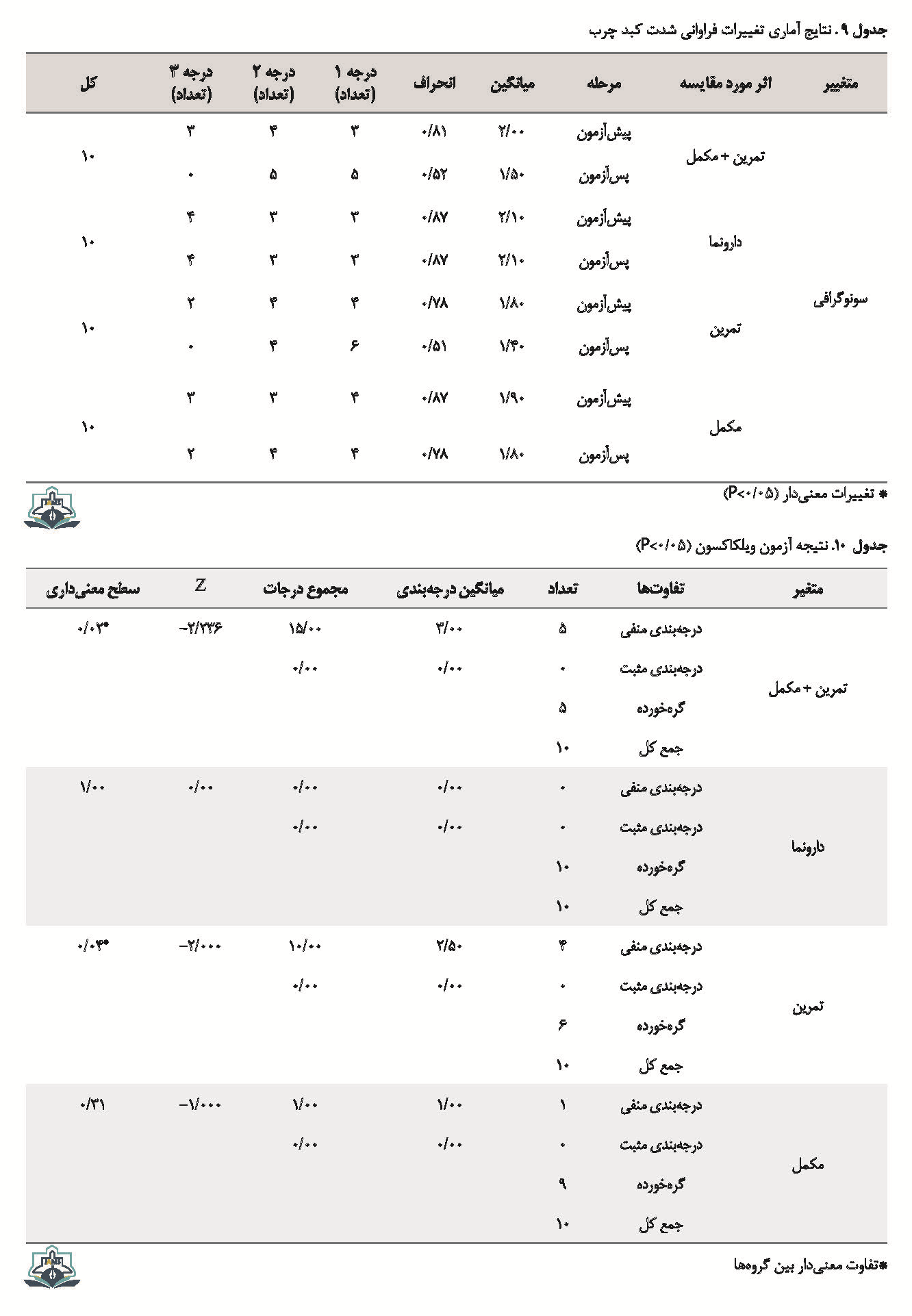
به دلیل اینکه دادههای حاصل از سونوگرافی اسمی بود، از شاخص گرایش مرکزی نما برای بررسی تغییرات چربی کبدی استفاده شد؛ همچنین نتایج تفکیک درجات کبد چرب در هر یک از گروههای چهارگانه و آزمون ویلکاکسون (توزیع دادهها با استفاده از آزمون شاپیروویک نرمال نبود) برای مقایسه قبل و بعد دادهها در جدول شماره 9 نشان داده شده است.
نتایج آزمون ویلکاکسون نشان داد که در گروه تمرین + مکمل و نیز گروه تمرین تفاوت معنیداری بین گروهها وجود دارد. میانگین درجهبندی بیماری در این دو گروه کاهش معنیداری داشت.
بحث
نتایج پژوهش حاضر نشان داد که 21 هفته تمرینات ترکیبی و مصرف مکمل یاری خرفه بر سطح چربی خون زنان چاق مبتلا به کبد چرب غیرالکلی اثر معناداری دارد. سطح کلسترول، LDL و تری گلیسیرید در گروههای تمرین + مکمل، گروه تمرین و گروه مکمل کاهش معنیداری و سطح HDL افزایش معنیداری داشت. در مقایسه بین گروهها مشاهده شد که تفاوت معنیداری بین گروههای تمرین + مکمل با سایر گروهها وجود داشت و در سایر گروهها علیرغم کاهش در سطح کلسترول، LDL و تری گلیسیرید از نظر آماری تغییرات معنیداری مشاهده نشد. این نتایج با نتایج پژوهش غفلتی و همکاران (2019) [15]، پاپولی و همکاران (2019) [17]، اسماعیلزاده و همکاران (2015) [14 ] همسو بود. غفلتی و همکاران (2019) نشان دادند که مصرف 10 گرم دانه خرفه با رژیم غذایی کمکالری موجب کاهش معنیداری در میزان غلظت سرمی قند خون ناشتا، شاخص مقاومت به انسولین، کلسترول تام و کلسترول لیپوپروتئین با چگالی کم میشود [15].
بحث
نتایج پژوهش حاضر نشان داد که 21 هفته تمرینات ترکیبی و مصرف مکمل یاری خرفه بر سطح چربی خون زنان چاق مبتلا به کبد چرب غیرالکلی اثر معناداری دارد. سطح کلسترول، LDL و تری گلیسیرید در گروههای تمرین + مکمل، گروه تمرین و گروه مکمل کاهش معنیداری و سطح HDL افزایش معنیداری داشت. در مقایسه بین گروهها مشاهده شد که تفاوت معنیداری بین گروههای تمرین + مکمل با سایر گروهها وجود داشت و در سایر گروهها علیرغم کاهش در سطح کلسترول، LDL و تری گلیسیرید از نظر آماری تغییرات معنیداری مشاهده نشد. این نتایج با نتایج پژوهش غفلتی و همکاران (2019) [15]، پاپولی و همکاران (2019) [17]، اسماعیلزاده و همکاران (2015) [14 ] همسو بود. غفلتی و همکاران (2019) نشان دادند که مصرف 10 گرم دانه خرفه با رژیم غذایی کمکالری موجب کاهش معنیداری در میزان غلظت سرمی قند خون ناشتا، شاخص مقاومت به انسولین، کلسترول تام و کلسترول لیپوپروتئین با چگالی کم میشود [15].
پاپولی و همکاران (2019) نیز کاهش معنیداری را در وزن، دور کمر، شاخص توده بدن، سطح سرمی LDL و کلسترول در زنان مبتلا به سندروم متابولیک مشاهد کردند، اما تغییرات در سطح سرمی HDL و تری گلیسیرید معنیدار نبود؛ همچنین مصرف دانه خرفه به مدت 12 هفته، کاهش معنیداری در غلظت قند خون ناشتا را به وجود آورد، اما اثر معنیداری بر فشارخون سیستولی و دیاستولی نداشت [17].
اسماعیلزاده و همکاران (2015) با انجام پژوهشی در خصوص اثر دانه خرفه بر وضعیت قند خون و پروفایل لیپیدی افراد مبتلا به دیابت نوع 2 به این نتیجه رسیدند که مصرف 10 گرم دانه خرفه به مدت 5 هفته در بیماران مبتلا به دیابت نوع 2 میتواند تری گلیسیرید را کاهش دهد، اما تأثیری روی HDL، LDL و کلسترول ندارد [14]. پژوهش ذکرشده با نتایج فرزانگی و همکاران (1393) [5] ناهمسو بود. از دلایل تناقض میتوان به شدت، نوع و مدت تمرین اشاره کرد؛ چراکه در پژوهش فرزانگی و همکاران از یک دوره تمرینات منتخب هوازی با شدت 50 تا 65 درصد حداکثر ضربان قلب به مدت 45 تا 60 دقیقه، 3 جلسه در هفته و به مدت 6 هفته استفاده شد که تفاوت معنیداری در پروفایل لیپیدی مشاهده نشد. مکانیسمهای احتمالی تأثیر فعالیتهای هوازی بر کاهش کلسترول خون در تحقیقات مختلف بهوفور یافت میشود و یک نتیجه کلی از تمام تحقیقات انجامشده در این زمینه این است که اکسیداسیون چربی در اثر افزایش فعالیت بدنی در ورزشهای هوازی بیشترین بازدهی را دارد و این اکسیداسیون چربی میتواند باعث کاهش تودههای چربی سایر اعضای بدن و همینطور کاهش کلسترول خون بیماران دچار سندروم کبد چرب شود [6].
از مکانیسمهای تأثیر تمرینات ورزشی هوازی بر تری گلیسیرید نیز میتوان به اکسیداسیون چربی اشاره کرد. هنگام فعالیت ورزشی با افزایش فعالیت سمپاتیکی، آزادسازی هورمون سوماتروپ ( هورمون رشد) از هیپوفیز قدامی و همچنین هورمون کورتیزول از قشر فوق کلیوی همزمان افزایش مییابد. افزایش غلظت اسیدهای چرب آزاد و اسیدهای آمینه در خون که با افزایش هورمون رشد و کورتیزول همراه است، سوبسترای لازم را برای عمل گلوکنئوژنز و سوختهای جایگزین را برای متابولیسم انرژی عضله اسکلای ( اسیدهای چرب آزاد) تأمین میکند [6]. بهطورکلی میتوان بیان کرد که مکانیسم تغییرات پروفایل چربیهای خون پس از تمرین ورزشی بهطورکامل معلوم نشده است.
اگرچه بسیاری از پیشرفتها ممکن است به تغییرات آنزیمی نسبت داده شود. از طرفی، عصاره خرفه حاوی مقادیر زیادی آلکالوئیدهای فنولیک است که سبب مهار سنتز کلسترول میشوند. به علاوه، در خرفه مقادیر زیادی ترکیبات آنتیاکسیدانی و چربیهای امگا- 3 و امگا -6 وجود دارد که سبب مهار پراکسیداسیون لیپیدی میشود. در مطالعات آمده است پلیفنلها و اسیدهای چرب امگا- 3 موجود در خرفه، مصرف انرژی در کبد چرب را افزایش میدهند؛ همچنین عصاره خرفه میتواند بیان استیل کوآنزیم A کربوکسیلاز و FAS آنزیمهای محدودکننده سرعت سنتز اسید چرب در کبد و بیان پروتئین متصلشونده به عنصر تنظیمکننده استرول را که بیان این آنزیمهای محدودکننده را کنترل میکند، کاهش دهد. از سوی دیگر، فیتواستروژنهای موجود در گیاه خرفه از طریق افزایش اسیدهای چرب غیراشباع باعث کاهش کلسترول و LDL-C میشوند. افزایش اسیدهای چرب غیراشباع به افزایش لپتین که یک عامل ضداشتهاست، منجر میشود. این فیتواستروژنها در مهار گیرندههای فاکتور رشد نیز نقش دارند. آلکالوئیدها نیز ازجمله ترکیبات دیگر این گیاه هستند که میتوانند سنتز کلسترول را مهار سازند [9].
بنابراین با توجه به نتیجه پژوهش حاضر و مطالب مطرحشده در زمینه اثر خرفه و تمرین ترکیبی به صورت مجزا میتوان بیان کرد که طراحی طرحی پژوهشی که به طور همزمان استفاده از مکمل خرفه و تمرین ترکیبی را دربرگیرد، میتواند در بهبود نیمرخ لیپیدی مفیدتر از انجام هر کدام بهتنهایی باشد. در پژوهش حاضر میزان تجمع چربی کبدی اندازهگیریشده به روش سونوگرافی در گروه تمرین + مکمل و گروه تمرین کاهش یافت. نتایج مطالعه حاضر با نتایج داوودی و همکاران (1391) [7] و شمسدینی و همکاران ( 2015) همسو بود [8]. مکانیسم مسئول کاهش چربی کبدی متعاقب تمرین ورزشی احتمالاً تغییر در تعادل انرژی، لیپیدهای گردش خون و حساسیت به انسولین (حساسیت به انسولین نقش مهمی در هومئوستاز چربی کبد دارد) است [5] که با کاهش معنادار چربی کبد پس از یک دوره تمرین هوازی در افراد مبتلا به کبد چرب همخوانی دارد. همچنین گزارش شده است که تمرین، مقاومت به انسولین را در بافت چربی بهبود میدهد که در تحویل اسیدهای چرب آزاد به کبد کاهش بیشتری ایجاد میکند و از طرف دیگر، بیوژنز میتوکندریابی را افزایش میدهد و درنتیجه بتا اکسیداسیون را بهبود میبخشد [5].
چاقی موجب کاهش توانایی اکسیداسیون چربی در شرایط ناشتا میشود که این وضعیت ذخیره چربی درونسلولی را افزایش میدهد. ازآنجاکه یکی از اثرات مثبت تمرین در افراد چاق افزایش اکسیداسیون چربی است، بنابراین یک توضیح احتمالی دیگر برای کاهش چربی کبدی پس از تمرین، افزایش ظرفیت اکسایشی عضله است که میتواند چربی درونسلولی را به عنوان سوخت در حین ورزش مصرف کند و موجب کاهش محتوای چربی کبدی شود [5]. چند مکانیسم دیگر نیز ازجمله اختلال در مسیرهای سیگنالینگ درونسلولی انسولین، افزایش اکسیداسیون اسیدهای چرب آزاد و کاهش تجمع چربیهای داخل سلولی در کبد، کاهش بتا اکسیداسیون، اختلال میتوکندریابی و استرس اکسیداتیو به عنوان مکانیسم اصلی کاهش چربی کبد پیشنهاد شده است [5].
با در نظر گرفتن مطالب گفتهشده و با توجه به اینکه این مقاله بخشی از پژوهشی انجامشده است (تأثیرگذاری تمرین و مکمل بهتنهایی در سایر پارامترهای بالینی مرتبط با کبد چرب به اثبات رسیده است)، لذا دور از انتظار نبود که تمرین به همراه مکمل، تأثیرگذاری بیشتری نسبت به استفاده از مکمل و تمرین بهتنهایی در متغیرهای فوق داشته باشد.
از ﻣﺤﺪودیتهای پژوهش ﺣﺎﺿﺮ ﻣﯽﺗﻮان به ﮐﻮﺗﺎه ﺑﻮدن ﻃـﻮل دوره ﻣﻄﺎﻟﻌـﻪ (12 هفته)، عدم تعیین میزان دقیق چربی کبد و آنزیمهای کبدی اشاره کرد که به دلیل سن بالای بیماران و عدم امکان ترمیم کامل سلولهای کبدی، تعیین میزان دقیق چربی کبد به روش بیوپسی امکانپذیر نبود؛ بنابراین ﭘﯿﺸﻨﻬﺎد ﻣﯽﺷﻮد ﮐﻪ ﻣﻄﺎﻟﻌﺎت آﺗﯽ ﺑﺎ دوره زﻣﺎﻧﯽ ﻃﻮﻻﻧﯽﺗﺮ، همچنین ﺑﻪ ﺻﻮرت ﻃﺮح پنجگروهه با در دست داشتن گروه کنترل و انجام بیوپسی کبد اﻧﺠﺎم ﺷـﻮد.
نتیجهگیری
درﻣﺠﻤﻮع، ﻧﺘﺎیﺞ پژوهش ﺣﺎﺿﺮ ﻧﺸـﺎن داد ﮐـﻪ ﺗﻤﺮیﻨـﺎت هوازی-ﻣﻘﺎوﻣﺘﯽ همراه ﺑـﺎ ﻣﺼـﺮف مکمل خرفه میتواند ﻣﻮﺟﺐ ﺑﻬﺒﻮد وضعیت تجمع چربی در کبد و غلظت سرمی چربیهای خون در زﻧﺎن چاق مبتلا به کبد چرب غیرالکلی ﺷﻮد؛ بنابراین با توجه به ترکیبات مختلف و اثرات مفید مکمل خرفه (کاهنده چربی خون، بهبوددهنده عملکرد کبد، خواص آنتیاکسیدانی) به همراه تمرینات ترکیبی، این دو با هم میتوانند به عنوان درمان کمکی در خصوص سایر پارامترهای بالینی مرتبط با بیماری کبد چرب (نشانههای بیوشیمیایی کبد و آنزیم های کبد) برای مبتلایان به این نوع بیماری استفاده شوند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این پژوهش با کد IR.IAU.RASHT.REC.1397.034 در کمیته اخلاق دانشگاه آزاد اسلامی واحد رشت تأیید شده است و دارای ثبت ﮐﺎرآزﻣــﺎیﯽ ﺑــﺎﻟﯿﻨﯽ ایﺮان به شماره IRCT20190309042987N1 است.
حامی مالی
این مقاله برگرفته از رساله خانم نرگس علی نیا دانشجوی دکتری گروه تربیت بدنی و علوم ورزشی دانشگاه آزاد واحد رشت می باشد که نویسنده در اجرای این پژوهش هیچ گونه کمک مالی از سازمان های خصوصی و دولتی دریافت نکرده است
مشارکت نویسندگان
تمامی نویسندگان معیارهای استاندارد نویسندگی بر اساس پیشنهادات کمیته بینالمللی ناشران مجلات پزشکی را دارا بودند.
تعارض منافع
در این پژوهش هیچ ﺗﻌﺎرضی در ﻣﻨﺎﻓﻊ وﺟﻮد ﻧﺪارد.
تشکر و قدردانی
پژوهش ﺣﺎﺿﺮ برگرفته از رساله دﻛﺘﺮی داﻧﺸﮕﺎه آزاد رﺷﺖ است ﻛﻪ ﺑﺎ هزینه شخصی اﻧﺠﺎم شده است. نویسندگان مقاله بدینوسیله از همه شرکتکنندگان که همکاری صمیمانهای در اجرای این پژوهش داشتند، سپاسگزاری میکنند.
از مکانیسمهای تأثیر تمرینات ورزشی هوازی بر تری گلیسیرید نیز میتوان به اکسیداسیون چربی اشاره کرد. هنگام فعالیت ورزشی با افزایش فعالیت سمپاتیکی، آزادسازی هورمون سوماتروپ ( هورمون رشد) از هیپوفیز قدامی و همچنین هورمون کورتیزول از قشر فوق کلیوی همزمان افزایش مییابد. افزایش غلظت اسیدهای چرب آزاد و اسیدهای آمینه در خون که با افزایش هورمون رشد و کورتیزول همراه است، سوبسترای لازم را برای عمل گلوکنئوژنز و سوختهای جایگزین را برای متابولیسم انرژی عضله اسکلای ( اسیدهای چرب آزاد) تأمین میکند [6]. بهطورکلی میتوان بیان کرد که مکانیسم تغییرات پروفایل چربیهای خون پس از تمرین ورزشی بهطورکامل معلوم نشده است.
اگرچه بسیاری از پیشرفتها ممکن است به تغییرات آنزیمی نسبت داده شود. از طرفی، عصاره خرفه حاوی مقادیر زیادی آلکالوئیدهای فنولیک است که سبب مهار سنتز کلسترول میشوند. به علاوه، در خرفه مقادیر زیادی ترکیبات آنتیاکسیدانی و چربیهای امگا- 3 و امگا -6 وجود دارد که سبب مهار پراکسیداسیون لیپیدی میشود. در مطالعات آمده است پلیفنلها و اسیدهای چرب امگا- 3 موجود در خرفه، مصرف انرژی در کبد چرب را افزایش میدهند؛ همچنین عصاره خرفه میتواند بیان استیل کوآنزیم A کربوکسیلاز و FAS آنزیمهای محدودکننده سرعت سنتز اسید چرب در کبد و بیان پروتئین متصلشونده به عنصر تنظیمکننده استرول را که بیان این آنزیمهای محدودکننده را کنترل میکند، کاهش دهد. از سوی دیگر، فیتواستروژنهای موجود در گیاه خرفه از طریق افزایش اسیدهای چرب غیراشباع باعث کاهش کلسترول و LDL-C میشوند. افزایش اسیدهای چرب غیراشباع به افزایش لپتین که یک عامل ضداشتهاست، منجر میشود. این فیتواستروژنها در مهار گیرندههای فاکتور رشد نیز نقش دارند. آلکالوئیدها نیز ازجمله ترکیبات دیگر این گیاه هستند که میتوانند سنتز کلسترول را مهار سازند [9].
بنابراین با توجه به نتیجه پژوهش حاضر و مطالب مطرحشده در زمینه اثر خرفه و تمرین ترکیبی به صورت مجزا میتوان بیان کرد که طراحی طرحی پژوهشی که به طور همزمان استفاده از مکمل خرفه و تمرین ترکیبی را دربرگیرد، میتواند در بهبود نیمرخ لیپیدی مفیدتر از انجام هر کدام بهتنهایی باشد. در پژوهش حاضر میزان تجمع چربی کبدی اندازهگیریشده به روش سونوگرافی در گروه تمرین + مکمل و گروه تمرین کاهش یافت. نتایج مطالعه حاضر با نتایج داوودی و همکاران (1391) [7] و شمسدینی و همکاران ( 2015) همسو بود [8]. مکانیسم مسئول کاهش چربی کبدی متعاقب تمرین ورزشی احتمالاً تغییر در تعادل انرژی، لیپیدهای گردش خون و حساسیت به انسولین (حساسیت به انسولین نقش مهمی در هومئوستاز چربی کبد دارد) است [5] که با کاهش معنادار چربی کبد پس از یک دوره تمرین هوازی در افراد مبتلا به کبد چرب همخوانی دارد. همچنین گزارش شده است که تمرین، مقاومت به انسولین را در بافت چربی بهبود میدهد که در تحویل اسیدهای چرب آزاد به کبد کاهش بیشتری ایجاد میکند و از طرف دیگر، بیوژنز میتوکندریابی را افزایش میدهد و درنتیجه بتا اکسیداسیون را بهبود میبخشد [5].
چاقی موجب کاهش توانایی اکسیداسیون چربی در شرایط ناشتا میشود که این وضعیت ذخیره چربی درونسلولی را افزایش میدهد. ازآنجاکه یکی از اثرات مثبت تمرین در افراد چاق افزایش اکسیداسیون چربی است، بنابراین یک توضیح احتمالی دیگر برای کاهش چربی کبدی پس از تمرین، افزایش ظرفیت اکسایشی عضله است که میتواند چربی درونسلولی را به عنوان سوخت در حین ورزش مصرف کند و موجب کاهش محتوای چربی کبدی شود [5]. چند مکانیسم دیگر نیز ازجمله اختلال در مسیرهای سیگنالینگ درونسلولی انسولین، افزایش اکسیداسیون اسیدهای چرب آزاد و کاهش تجمع چربیهای داخل سلولی در کبد، کاهش بتا اکسیداسیون، اختلال میتوکندریابی و استرس اکسیداتیو به عنوان مکانیسم اصلی کاهش چربی کبد پیشنهاد شده است [5].
با در نظر گرفتن مطالب گفتهشده و با توجه به اینکه این مقاله بخشی از پژوهشی انجامشده است (تأثیرگذاری تمرین و مکمل بهتنهایی در سایر پارامترهای بالینی مرتبط با کبد چرب به اثبات رسیده است)، لذا دور از انتظار نبود که تمرین به همراه مکمل، تأثیرگذاری بیشتری نسبت به استفاده از مکمل و تمرین بهتنهایی در متغیرهای فوق داشته باشد.
از ﻣﺤﺪودیتهای پژوهش ﺣﺎﺿﺮ ﻣﯽﺗﻮان به ﮐﻮﺗﺎه ﺑﻮدن ﻃـﻮل دوره ﻣﻄﺎﻟﻌـﻪ (12 هفته)، عدم تعیین میزان دقیق چربی کبد و آنزیمهای کبدی اشاره کرد که به دلیل سن بالای بیماران و عدم امکان ترمیم کامل سلولهای کبدی، تعیین میزان دقیق چربی کبد به روش بیوپسی امکانپذیر نبود؛ بنابراین ﭘﯿﺸﻨﻬﺎد ﻣﯽﺷﻮد ﮐﻪ ﻣﻄﺎﻟﻌﺎت آﺗﯽ ﺑﺎ دوره زﻣﺎﻧﯽ ﻃﻮﻻﻧﯽﺗﺮ، همچنین ﺑﻪ ﺻﻮرت ﻃﺮح پنجگروهه با در دست داشتن گروه کنترل و انجام بیوپسی کبد اﻧﺠﺎم ﺷـﻮد.
نتیجهگیری
درﻣﺠﻤﻮع، ﻧﺘﺎیﺞ پژوهش ﺣﺎﺿﺮ ﻧﺸـﺎن داد ﮐـﻪ ﺗﻤﺮیﻨـﺎت هوازی-ﻣﻘﺎوﻣﺘﯽ همراه ﺑـﺎ ﻣﺼـﺮف مکمل خرفه میتواند ﻣﻮﺟﺐ ﺑﻬﺒﻮد وضعیت تجمع چربی در کبد و غلظت سرمی چربیهای خون در زﻧﺎن چاق مبتلا به کبد چرب غیرالکلی ﺷﻮد؛ بنابراین با توجه به ترکیبات مختلف و اثرات مفید مکمل خرفه (کاهنده چربی خون، بهبوددهنده عملکرد کبد، خواص آنتیاکسیدانی) به همراه تمرینات ترکیبی، این دو با هم میتوانند به عنوان درمان کمکی در خصوص سایر پارامترهای بالینی مرتبط با بیماری کبد چرب (نشانههای بیوشیمیایی کبد و آنزیم های کبد) برای مبتلایان به این نوع بیماری استفاده شوند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این پژوهش با کد IR.IAU.RASHT.REC.1397.034 در کمیته اخلاق دانشگاه آزاد اسلامی واحد رشت تأیید شده است و دارای ثبت ﮐﺎرآزﻣــﺎیﯽ ﺑــﺎﻟﯿﻨﯽ ایﺮان به شماره IRCT20190309042987N1 است.
حامی مالی
این مقاله برگرفته از رساله خانم نرگس علی نیا دانشجوی دکتری گروه تربیت بدنی و علوم ورزشی دانشگاه آزاد واحد رشت می باشد که نویسنده در اجرای این پژوهش هیچ گونه کمک مالی از سازمان های خصوصی و دولتی دریافت نکرده است
مشارکت نویسندگان
تمامی نویسندگان معیارهای استاندارد نویسندگی بر اساس پیشنهادات کمیته بینالمللی ناشران مجلات پزشکی را دارا بودند.
تعارض منافع
در این پژوهش هیچ ﺗﻌﺎرضی در ﻣﻨﺎﻓﻊ وﺟﻮد ﻧﺪارد.
تشکر و قدردانی
پژوهش ﺣﺎﺿﺮ برگرفته از رساله دﻛﺘﺮی داﻧﺸﮕﺎه آزاد رﺷﺖ است ﻛﻪ ﺑﺎ هزینه شخصی اﻧﺠﺎم شده است. نویسندگان مقاله بدینوسیله از همه شرکتکنندگان که همکاری صمیمانهای در اجرای این پژوهش داشتند، سپاسگزاری میکنند.
References
Sahebkar Khorasani MS, Azizi H, Yousefi M, Salari R, Bahrami-Taghanaki HR, Behravanrad P. [An evidence based review on integrative medicine in weight control (Persian)]. Complement Med J. 2017; 7(1):1828-50. http://cmja.arakmu.ac.ir/article-1-453-en.html
Safarpor M, Kohan L, Porkhajeh A. [Comparative study of anthropometric parameters in non-alcoholic fatty liver disease patients and healthy subjects (Persian)]. J Sabzevar Univ Med Sci. 2015; 22(3):225-31. http://jsums.medsab.ac.ir/article_555.html
Bahmanabadi Z, Ebrahimi-Mamghani M, Arefhosseini SR. [Comparision of low-calorie diet with and without sibutramine on body weight and liver function of patients with non-alcoholic fatty liver disease (Persian)]. Armaghan-e Danesh. 2011; 16(2):101-10. http://armaghanj.yums.ac.ir/article-1-378-en.html
Ghaemi AR, Taleban FA, Hekmatdoost A, Rafiei AR, Hosseini V, Amiri Z, et al. [Effect of weight reduction diet on non-alcoholic fatty liver disease (Persian)]. Iran J Nutr Sci Food Technol. 2013; 8(2):123-34. http://nsft.sbmu.ac.ir/article-1-1391-fa.html
Kaki A, Galedari M. [The effect of 12 weeks high intensity interval training and resistance training on liver fat, liver enzymes and insulin resistance in men with nonalcoholic fatty liver (Persian)]. Jundishapur Sci Med J. 2017; 16(5):493-503. [DOI:10.22118/JSMJ.2017.53990]
Davoodi M, Moosavi H, Nikbakht M. [The effect of eight weeks selected aerobic exercise on liver parenchyma and liver enzymes (AST, ALT) of fat liver patients (Persian)]. J Shahrekord Univ Med Sci. 2012; 14(1):84-90. http://journal.skums.ac.ir/article-1-1054-en.html
Nikroo H, Nematy M, Sima HR, Attarzade Hosseini SR, Pezeshki Rad M, Esmaeilzadeh A, et al. [Therapeutic effects of aerobic exercise and low-calorie diet on nonalcoholic steatohepatitis (Persian)]. Govaresh J. 2013; 17(4):245-51. http://govaresh.org/index.php/dd/article/view/1096
Shamsoddini A, Sobhani V, Ghamar Chehreh ME, Alavian SM, Zaree A. Effect of aerobic and resistance exercise training on liver enzymes and hepatic fat in Iranian men with nonalcoholic fatty liver disease. Hepat Mon. 2015; 15(10):e31434. [DOI:10.5812/hepatmon.31434] [PMID] [PMCID]
Changizi-Ashtiyani S, Zarei A, Taheri S, Rasekh F, Ramazani M. The effects of Portulaca oleracea alcoholic extract on induced hypercholesteroleomia in rats. Zahedan J Res Med Sci. 2012; 15(6):e92959. http://sites.kowsarpub.com/zjrms/articles/92959.html
Moosavi-Sohroforouzani A, Ganbarzadeh M. [Reviewing the physiological effects of aerobic and resistance training on insulin resistance and some biomarkers in non-alcoholic fatty liver disease (Persian)]. Feyz. 2016; 20(3):282-96. http://feyz.kaums.ac.ir/article-1-3091-en.html
Li J, Wang F, Chen K, Xia Y, Lu J, Zhou Y, et al. Effects of physical activity on liver function in patients with non-alcoholic fatty liver disease: A meta-analysis. SOJ Immunol. 2015; 3(5):1-6. [DOI:10.15226/2372-0948/3/5/00143]
Salehi A, Farzanegi P. [Effect of 8 weeks of resistance training with and without portulacalo seeds on some of liver injury markers in women with diabetes type 2 (Persian)]. Stud Med Sci. 2015; 25(11):968-78. http://umj.umsu.ac.ir/article-1-2603-en.html
El-Sayed MI. Effects of Portulaca oleracea L. seeds in treatment of type-2 diabetes mellitus patients as adjunctive and alternative therapy. J Ethnopharmacol. 2011; 137(1):643-51. [DOI:10.1016/j.jep.2011.06.020] [PMID]
Dehghan F, Soori R, Gholami K, Abolmaesoomi M, Yusof A, Muniandy S, et al. Purslane (Portulaca oleracea) seed consumption and aerobic training improves biomarkers associated with atherosclerosis in women with Type 2 Diabetes (T2D). Sci Rep. 2016; 6:37819. [DOI:10.1038/srep37819] [PMID] [PMCID]
Gheflati A, Adelnia E, Nadjarzadeh A. The clinical effects of purslane (Portulaca oleracea) seeds on metabolic profiles in patients with nonalcoholic fatty liver disease: A randomized controlled clinical trial. Phytother Res. 2019; 33(5):1501-9. [DOI:10.1002/ptr.6342] [PMID]
Esmaillzadeh A, Zakizadeh E, Faghihimani E, Gohari M, Jazayeri S. The effect of purslane seeds on glycemic status and lipid profiles of persons with type 2 diabetes: A randomized controlled cross-over clinical trial. J Res Med Sci. 2015; 20(1):47-53. [PMID] [PMCID]
Papoli M, Pishdad S, Nadjarzadeh A, Hosseinzadeh M. Effects of consuming purslane seed powder on indicators of metabolic syndrome in women: A randomized clinical trial. Prog Nutr. 2019; 21(Suppl. 1):329-35. [DOI:10.23751/pn.v21i1-S.6210]
Behzadimoghadam M, Galedari M, Motalebi L. [The effect of eight weeks resistance training and low-calorie diet on plasma levels of liver enzymes and liver fat in Non-Alcoholic Fatty Liver Disease (NAFLD) (Persian)]. Iran J Nutr Sci Food Technol. 2018; 12(4):25-32. http://nsft.sbmu.ac.ir/article-1-2356-en.html
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |