دوره 22، شماره 6 - ( بهمن و اسفند 1398 )
جلد 22 شماره 6 صفحات 203-192 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Zamani N, Moazedi A A. The Effects of Co-Administration of Memantine And Vitamin D on Spatial Learning and Memory Impairment in Adult Male Rats Model of Alzheimer’s Disease. J Arak Uni Med Sci 2020; 22 (6) :192-203
URL: http://jams.arakmu.ac.ir/article-1-6147-fa.html
URL: http://jams.arakmu.ac.ir/article-1-6147-fa.html
زمانی نسترن، معاضدی احمد علی. اثرات تجویز توأم ممانتین و ویتامین D بر اختلالات یادگیری و حافظه فضایی در مدل بیماری آلزایمر موشهای صحرایی نر بالغ. مجله دانشگاه علوم پزشكي اراك. 1398; 22 (6) :192-203
1- گروه زیست شناسی، دانشکده علوم، دانشگاه پیام نور، تهران، ایران. ، na_zamani2000@yahoo.com
2- گروه زیست شناسی، دانشکده علوم، دانشگاه شهید چمران اهواز، اهواز، ایران.؛ مرکز تحقیقات سلولهای بنیادی و فناوری ترانسژنیک، دانشگاه شهید چمران اهواز، اهواز، ایران.
2- گروه زیست شناسی، دانشکده علوم، دانشگاه شهید چمران اهواز، اهواز، ایران.؛ مرکز تحقیقات سلولهای بنیادی و فناوری ترانسژنیک، دانشگاه شهید چمران اهواز، اهواز، ایران.
متن کامل [PDF 2780 kb]
(1307 دریافت)
| چکیده (HTML) (2978 مشاهده)
در بررسی اثرات ویتامین D، ممانتین و تأثیر توأم آنها بر یادگیری و حافظه فضایی نتایج آنالیز آماری نشاندهنده افزایش میانگین تعداد پاسخ صحیح در روزهای اول (0/05˂P)، دوم (0/05˂P)، سوم (0/01˂P)، چهارم (0/05˂P) و پنجم (0/05˂P) آموزش در گروه تخریب + ویتامین D، در روزهای دوم (0/05˂P)، سوم (0/05˂P) و چهارم (0/05˂P) آموزش در گروه تخریب + ممانتین و در روزهای اول (0/01˂P)، دوم (0/001˂P)، سوم (0/001˂P)، چهارم (0/01˂P) و پنجم (0/05˂P) آموزش در گروه تخریب + ویتامین D + ممانتین در مقایسه با گروه تخریب است که نتایج این بررسی نشاندهنده اثرات افزایشی تأثیر توأم ویتامین D و ممانتین بر میانگین تعداد پاسخ صحیح در روزهای اول، دوم، سوم و چهارم آموزش است. علاوه بر این در گروههای مورد بررسی بین میانگین تعداد پاسخ صحیح در روز پنجم آموزش با آزمون فراخوانی حافظه در روز سیام اختلاف معنیداری مشاهده نشد (تصویر شماره 3).
بحث
با توجه به اینکه اثرات ممانتین و ویتامین D بهتنهایی در درمان اختلالات شناختی در بیماران مبتلا به آلزایمر ناکافی است که این امر در یافتههای این پژوهش نیز نشان داده شده است در مطالعه حاضر امکان افزایش اثربخشی مقادیر درمانی ممانتین تحت تأثیر ویتامین D بررسی شده است. بدین منظور مقادیر با تأثیر کم این دو ماده انتخاب و تأثیر توأم آنها بر یادگیری و حافظه فضایی در گروههای با تخریب الکتریکی دوطرفه NBM مورد بررسی قرار گرفت. یافتههای این مطالعه نشان میدهند که درمان توأم ویتامین D و ممانتین از طریق تزریق داخل صفاقی ویتامین D به مدت 10 روز با شروع سه روز قبل از تخریب NBM و القای مدل بیماری آلزایمر و تزریق داخل صفاقی ممانتین به مدت پنج روز با شروع هفت روز پس از تخریب NBM نسبت به تجویز هریک از این دو بهتنهایی دارای تأثیر بیشتری در بهبود اختلال یادگیری و حافظه فضایی در موشهای مدل بیماری آلزایمر است. NBM از هستههای کولینرژیک قاعده مغز جلویی است [3] که در مطالعه حاضر تخریب الکتریکی دوطرفه آن منجر به کاهش معنیدار فرایند یادگیری و حافظه فضایی شد (تصویر شماره 1). در همین راستا ژائو و همکاران نیز نشان دادهاند که تخریب NBM به وسیله ایبوتنیک اسید منجر به اختلال حافظه در آزمون ماز آبی موریس و کاهش فعالیت کولین استیل ترانسفراز (ChAT) در قشر فرونتال و هیپوکامپ میشود [17]. علاوه بر این نشان داده شده است که تخریب دوطرفه NBM به وسیله ایبوتنیک اسید منجر به کاهش سطوح استیل کولین، کولین استراز و کولین استیل ترانسفراز در قشر مغز و اختلال حافظه فضایی در آزمون ماز آبی موریس و حافظه شناختی در آزمون شناخت اشیای جدید میشود [18] که این نتایج همراستا با نتایج این پژوهش هستند.
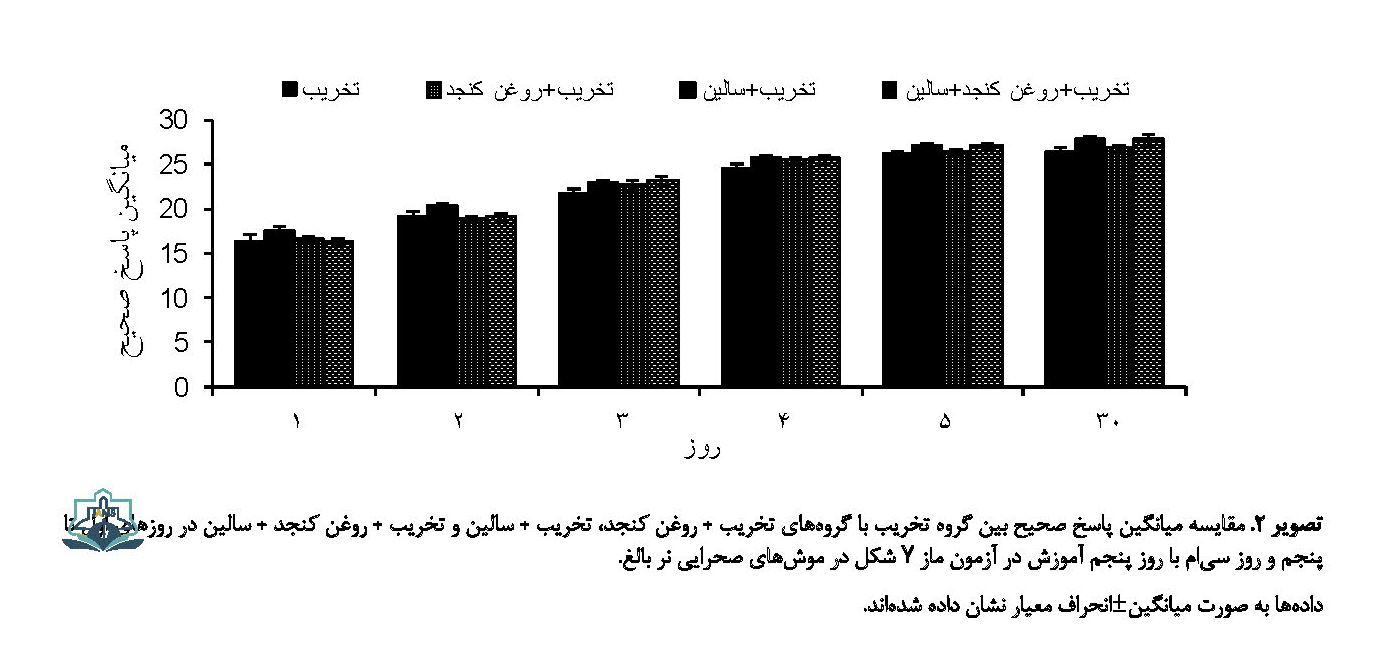
در این بررسی اختلاف معنیداری در یادگیری فضایی موشهای صحرایی در گروههای کنترل و شاهد تخریب مشاهده نشد که نشان میدهد مراحل مختلف بیهوشی، جراحی و ورود الکترود به NBM بدون ایجاد تخریب اثری بر یادگیری فضایی در موشهای صحرایی ندارد (تصویر شماره 1). همچنین مقایسه نتایج بین گروههای تخریب، تخریب + روغن کنجد، تخریب + سالین و تخریب + روغن کنجد + سالین نشان داد که روغن کنجد (حلال ویتامین D)، سالین (حلال ممانتین) و تجویز توأم آنها هیچگونه تأثیری بر یادگیری فضایی ندارد (تصویر شماره 2).
علاوه بر این یافتههای این مطالعه نشان میدهد که ویتامین D و ممانتین در تجویز توأم دارای اثرات همافزایی بر بهبود یادگیری فضایی در موشهای صحرایی با تخریب الکتریکی دوطرفه NBM هستند (تصویر شماره 3). مقادیر ویتامین D و ممانتین بر اساس مطالعات انجامشده پیشین انتخاب شدند [14 ،13]. در همین راستا در مطالعات چن و همکاران نیز نشان داده شده است که در موشهای ترانسژنیک مدل آلزایمر اسیدفولیک موجب افزایش اثرات ممانتین در محافظت عصبی نورونهای ناحیه CA1 هیپوکامپ و یادگیری فضایی در ماز آبی موریس میشود [19].
در مطالعات احمدی زهرانی و همکاران نیز تأثیر ممانتین در بهبود نقایص شناختی اختلالات خاص یادگیری که یک اختلال عصبی رشدی است نشان داده شد [20]. از طرف دیگر در مطالعات دی و همکاران نشان داده شد که 17-β- استرادیول نیز که همانند ویتامین D دارای اثرات محافظت عصبی است در درمان توأم با ممانتین در مدل آسیب مغزی تروماتیک منجر به کاهش دژنراسیون نورونی و افزایش بقاء نورونها میشود [21]. نتایج مطالعات آنوایلر و همکاران در شرایط in vitro نیز نشاندهنده مهار دژنراسیون آکسونی القاشده به وسیله گلوتامات و Aβ در نورونهای قشری موشهای صحرایی تحت درمان توأم ممانتین و ویتامین D هستند [22] که با توجه به نتایج این مطالعه میتوان نتیجه گرفت که درمان توأم ممانتین و ویتامین D مؤثرتر از تجویز هریک از این دو ماده بهتنهایی است.
مکانیسم برهمکنش ممانتین و ویتامین D در مدل بیماری آلزایمر از طریق تخریب NBM تاکنون مورد بررسی قرار نگرفته است، اما مطالعات متعددی در خصوص مکانیسمهای عمل هریک از این دو بهتنهایی انجام شده است. به عنوان مثال نتایج یک مطالعه نشاندهنده اثرات ممانتین بر افزایش سطوح استیل کولین خارج سلولی در هیپوکامپ هستند [23]. همچنین در مطالعات اهالاینن روی موشهای صحرایی با تخریب فیمبریافورنیکس افزایش ناچیز سطوح استیل کولین نئوکورتکس و هیپوکامپ تحت درمان مزمن ممانتین و افزایش معنیدار آن تحت درمان حاد با ممانتین نشان داده شده است که با توجه به اینکه درمان مزمن ممانتین در بررسیهای رفتاری نسبت به درمان حاد آن دارای تأثیر بیشتری بر بهبود یادگیری و حافظه است، به نظر میرسد که اثرات درمانی ممانتین بر بهبود حافظه طولانیمدت دارای مکانیسمهای متفاوتی نسبت به اثرات درمانی آن بر بهبود حافظه کوتاهمدت افزایش سطوح استیل کولین در قشر و هیپوکامپ است [5]. علاوه بر این نشان داده شده است که ممانتین در غلظتهای درمانی موجب محافظت در برابر آسیب نورونی و آپوپتوز القاشده به وسیله تزریق مستقیم Aβ1-40 به هیپوکامپ میشود [24]. علاوه بر این، تأثیر ممانتین بر کاهش سطوح TNF-α در هیپوکامپ و کاهش سطوح IL-1β در قشر و هیپوکامپ در مدل آلزایمر القاشده به وسیله تزریق داخل هیپوکامپی Aβ نیز نشان داده شده است [25]. نتایج حاصل از مطالعه ما نیز از نظر تأثیر ممانتین بر بهبود یادگیری و حافظه با موارد پیشگفته همخوانی داشت.
از طرف دیگر بهبود نوروژنز و اعمال شناختی در موشهای ترانسژنیک مدل آلزایمر تحت درمان با مکمل ویتامین D نیز نشان داده شده است [26]. در مطالعات یامینی و همکاران نشان داده شد که پیش درمان با ویتامین D به طور مؤثری موجب بهبود حافظه فضایی در ماز آبی موریس میشود. علاوه بر این در این مطالعه کاهش استرس اکسیداتیو و افزایش سطوح استیل کولین استراز در کورتکس مغز و هیپوکامپ موشهای صحرایی مدل آلزایمر نیز تحت پیش درمان با ویتامین D بهبود یافت [27].
در بررسیهای پیوش و همکاران نیز مکمل ویتامین D3 موجب بازگشت تغییرات ایجادشده در گیرندههای کولینرژیک و فعالیت استیل کولین استراز در موشهای صحرایی دیابتیشده توسط STZ شد [28]. علاوه بر این، استفاده از مکمل ویتامین D در افراد میانسال مبتلا به کمبود این ویتامین، منجر به افزایش سطوح پلاسمایی Aβ40 شد که این نتایج نشاندهنده تأثیر ویتامین D بر کاهش Aβ در بافت مغزی [29] از طریق تحریک فاگوسیتوز Aβ توسط ماکروفاژهای نوع I و II، بازجذب و کلیرانس Aβ هستند [11].
در همن راستا در مطالعات بریونز و درویش در سال 2012 کاهش Aβ تحت تأثیر درمان با ویتامین D در موشهای صحرایی مسن نشان داده شد [30]. همچنین برخی مطالعات اثرات ضدالتهابی ویتامین D و تأثیر آن را بر بازگشت تغییرات التهابی مرتبط با سن در هیپوکامپ موشهای صحرایی نشان میدهند که در این زمینه سرکوب سایتوکینهای پیشالتهابی در مغز را میتوان به عنوان مکانیسمی برای اعمال محافظت عصبی ویتامین D در نظر گرفت [10 ،9]. بنابراین به نظر میرسد که در درمان توأم ممانتین و ویتامین D، ویتامین D با بهبود نوروژنز و اعمال شناختی، افزایش محافظت عصبی، کاهش التهاب و تنظیم اعمال کولینرژیک موجب بهبود حافظه و یادگیری در موشهای صحرایی مدل آلزایمر و تحت تیمار با ممانتین میشود.
نتیجهگیری
در این مطالعه از تخریب الکتریکی دوطرفه NBM به عنوان مدلی جهت القای بیماری آلزایمر در موشهای صحرایی استفاده شده است. با توجه به نتایج این پژوهش، تجویز توأم ویتامینD و ممانتین در مقادیر کم نسبت به تجویز هریک از این دو بهتنهایی دارای تأثیر بیشتری بر بهبود یادگیری و حافظه فضایی در موشهای مدل آلزایمر است.
پیشنهاد میشود که برای مطالعات بیشتر در این زمینه اثرات تجویز توأم ممانتین و ویتامین D بر سطوح پلاسمایی Aβ و همچنین استرس اکسیداتیو و فعالیت استیل کولین استراز در بافت مغزی موشهای صحرایی مدل آلزایمر بررسی شود.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این مطالعه با کد اخلاق EE/ 97, 24, 3061243/scu.ac.irتوسط کمیته اخلاق پژوهشی دانشگاه شهید چمران اهواز به تصویب رسیده است.
حامی مالی
این مقاله از حمایت مالی دانشگاه شهید چمران اهواز برخوردار بوده است
مشارکت نویسندگان
تمامی نویسندگان در نگارش این مقاله به یک اندازه مشارکت داشتهاند.
تعارض منافع
نویسندگان اعلام میدارند که هیچگونه تضاد منافعی در پژوهش حاضر وجود ندارد.
تشکر و قدردانی
بدینوسیله نویسندگان مراتب تشکر و قدردانی خود را از معاونت پژوهشی دانشگاه شهید چمران اهواز به جهت همکاری و مساعدت در انجام این پروژه علمی- پژوهشی اعلام می دارند.
متن کامل: (28189 مشاهده)
مقدمه
بیماری آلزایمر شایعترین شکل دمانس است که به واسطه رسوبات خارج سلولی پلاکهای آمیلوئید بتا و تجمعات داخل سلولی کلافههای نروفیبریلاری که از عوامل سمیت عصبی و فقدان سیناپسی هستند منجر به نورودژنراسیون میشود [1]. علاوه بر این، اختلال در نورونهای کولینرژیک یا گیرندههای پس سیناپسی استیل کولین، مستقیماً با نقص شناختی ایجادشده در بیماری آلزایمر در ارتباط هستند. نشان داده شده است که استیل کولین و سیگنالینگ کولینرژیک جهت اعمال شناختی از جمله یادگیری و حافظه ضروری هستند [2]. اختلال در عملکرد و یا فقدان گروههای سلولی کولینرژیک در قاعده مغز جلویی از جمله هستههای قاعدهای مگنوسلولاریس در جوندگان و یا معادل آن هستههای قاعدهای مینرت در انسان از اولین وقایع پاتولوژیک در پاتوژنز بیماری آلزایمر هستند [3].
ممانتین آنتاگونیست غیررقابتی، گیرنده NMDA است که به صورت بالینی جهت درمان بیماری آلزایمر مورد استفاده قرار میگیرد. تحقیقات پیشین تأثیر ممانتین را بر افزایش سطوح خارج سلولی استیل کولین در هسته اکومبنس، نواحی تگمنتال شکمی [4] و هیپوکامپ [5] و همچنین بهبود نقص حافظه فضایی در موشهای مدل ترانسژنیک بیماری آلزایمر نشان دادهاند [6]. علاوه براین نشان داده شده است که درمان مزمن ممانتین به مدت 28 روز با کاهش آستروگلیوزیس، افزایش غلظتهای BDNF و GDNF، موجب محافظت عصبی، کاهش حجم آسیب و کاهش آتروفی مغزی ثانویه میشود [7].
برخی شواهد نقش مواد غذایی را در پیشگیری و یا کاهش ریسک ابتلا به بیماری آلزایمر نشان میدهند. با توجه به اینکه التهاب و آسیب اکسیداتیو نورونها میتواند عامل مرگ نورونها در بیماری آلزایمر باشد، احتمالاً مواد غذایی با ویژگیهای ضدالتهابی یا آنتیاکسیدانی خود نقش مهمی در کاهش ابتلا و مهار پیشرفت زوال عقل دارند [8]. برخی شواهد تأثیر ویتامین D را به عنوان یک عامل ضدالتهابی نشان دادهاند [9] که سرکوب سایتوکینهای پیشالتهابی در مغز احتمالاً مکانیسمی برای اعمال محافظت عصبی به وسیله ی ویتامین D است [10]. همچنین نشان داده شده است که ویتامین D در بیماران مبتلا به آلزایمر موجب تحریک فاگوسیتوز Aβ در ماکروفاژهای نوع I و II، بازجذب و کلیرانس Aβ میشود [11]. علاوه بر این، تأثیر ویتامین D بر افزایش آزادسازی فاکتور رشد عصب در نورونهای هیپوکامپ موشهای صحرایی نیز نشان داده شده است [12].
با توجه به تأثیر ممانتین در افزایش غلظت سیناپسی استیل کولین و نقش آن در محافظت عصبی و همچنین با در نظر گرفتن تأثیر ویتامین D در افزایش آزادسازی NGF، سرکوب سایتوکینهای پیشالتهابی و نیز اثرات آنتیاکسیدانی آن، در مطالعه حاضر بر آن شدیم تا پس از القای مدل آلزایمر از طریق تخریب الکتریکی دوطرفه NBM اثرات همافزایی ممانتین و ویتامین D را بر بهبود اختلالات یادگیری و حافظه فضایی مورد بررسی قرار دهیم.
مواد و روشها
در این مطالعه تجربی از موشهای صحرایی نر بالغ از نژاد ویستار با محدوده وزنی 20±200 گرم استفاده شد. موشها در گروههای چهارتایی در هر قفس، در خانه حیوانات با درجه حرارت کنترلشده (24-20 درجه سانتیگراد) و تحت چرخه روشنایی تاریکی 12ساعته نگهداری شدند و آب و غذا به مقدار کافی در دسترس داشتند. آزمایشات رفتاری در دوره روشنایی و با استفاده از دستگاه ماز Y شکل انجام گرفت. مواد مورد استفاده ممانتین، ویتامین D و روغن کنجد بودند که از شرکت سیگما تهیه شدند. در روز آزمایش غلظتهای مورد نظر ممانتین و ویتامین D به ترتیب توسط حلال سالین 0/9 درصد و روغن کنجد به صورت روزانه آماده میشد. موشها به طور تصادفی به 9 گروه (7=n) تقسیم شدند.
گروه کنترل: گروهی که تحت هیچگونه تزریق یا جراحی قرار نگرفتند. گروه ضایعهدیده (آلزایمری): گروهی که در آنها تحت عمل جراحی استرئوتاکسیک الکترود تخریب به صورت دوطرفه وارد NBM شد و با عبور جریان الکتریکی عمل تخریب انجام شد. گروه شاهد تخریب: گروهی که تحت جراحی و ورود الکترود به NBM بدون تخریب این هسته قرار گرفتند. گروه تخریب + روغن کنجد: گروهی که تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند و روغن کنجد (حلال ویتامین D) را به میزان 0/2 میلیلیتر به مدت 10 روز با شروع سه روز قبل از تخریب NBM به صورت تزریق داخل صفاقی دریافت کردند. گروه تخریب + سالین: گروهی که تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند و یک هفته بعد، سالین (حلال ممانتین) را به میزان 0/2 میلیلیتر به مدت پنج روز نیمساعت قبل از آموزش به صورت تزریق داخل صفاقی دریافت کردند. گروه تخریب + روغن کنجد + سالین: گروهی که تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند. این گروه روغن کنجد (حلال ویتامین D) را به مدت 10 روز با شروع سه روز قبل از تخریب و سالین (حلال ممانتین) را به میزان 0/2 میلیلیتر به مدت پنج روز نیمساعت قبل از آموزش به صورت تزریق داخل صفاقی دریافت کردند.
گروه تخریب+ ویتامین D: این گروه تحت عمل جراحی تخریب الکتریکی دو طرفه ی NBM قرار گرفتند و یک هفته بعد پنج میکروگرم بر کیلوگرم ویتامین D را به مدت 10 روز با شروع 3 روز قبل از تخریب به صورت تزریق داخل صفاقی دریافت کردند [13]. گروه تخریب + ممانتین: این گروه تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند و یک هفته بعد سه میلیگرم بر کیلوگرم ممانتین را به مدت پنج روز نیمساعت قبل از آموزش به صورت تزریق داخلصفاقی دریافت کردند [14]. تخریب + ویتامینD + ممانتین: گروهی که تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند. این گروه پنج میکروگرم بر کیلوگرم ویتامین D را به مدت 10 روز با شروع سه روز قبل از تخریب و سه میلیگرم بر کیلوگرم ممانتین را به مدت پنج روز نیمساعت قبل از آموزش به صورت تزریق داخل صفاقی دریافت کردند. گروه کنترل و سایر گروهها یک هفته بعد از جراحی (دوره بهبودی) به مدت پنج روز در دستگاه ماز Y شکل آموزش دیدند.
موشها جهت تخریب الکتریکی هسته NBM تحت بیهوشی عمومی با تزریق داخل صفاقی مخلوطی متشکل از 78 میلیگرم بر کیلوگرم کلروهیدرات کتامین 10 درصد و سه میلیگرم بر کیلوگرم زایلازین دو درصد قرار گرفتند [15] و سپس در دستگاه استرئوتاکسی (Stoelting, USA) ثابت شدند. میله دندانی 3/3 میلیمتر زیر صفر افقی قرار گرفت تا مطابق اطلس، وضعیت مناسب جمجمه حاصل شود. سپس موهای پشت سر حیوان از ناحیه بین چشمها تا گوشها تراشیده و پوست این ناحیه ضدعفونی شد. با کمک اسکالپل یک برش طولی در پوست ناحیه پشت سر حیوان داده شد و بعد از کنارزدن بافتهای پیوندی، محل موردنظر با نرمال سالین تمیز شد تا درزهای جمجمه نمایان شوند. مختصات مورد استفاده برای NBM طبق اطلس پاکسینوس و واتسون عبارت بود از: 3/1AP=- از برگما، 8/2ML=± از خط وسط و 6/7DV=- از سطح سخت شامه.
با استفاده از دستگاه ایجادکننده ضایعه (Lesion Making Device, UGO Basile) پس از قرارگرفتن الکترود در نقطه مورد نظر با عبور جریان الکتریکی مستقیم با شدت 5/0 میلیآمپر به مدت سه ثانیه [15] NBM در هر دو نیمکره مغزی به صورت الکتریکی تخریب شد و مدل آلزایمر ایجاد شد.
جهت بررسی روند یادگیری و حافظه در مدلهای آزمایشگاهی از دو روش تنبیه (دریافت شوک یا احساس ناخوشایند) و تشویق (دریافت پاداش مثل آب و غذا) استفاده میشود که با توجه به تداخل احتمالی برخی داروها در مکانیسم اشتها، به نظر میرسد برای بررسی تأثیر داروها بر روند یادگیری، روش تنبیه مناسبتر است. با توجه به اینکه هیپوکامپ در حافظه فضایی نقش عمدهای دارد در این تحقیق از دستگاه ماز Y شکل به منظور بررسی یادگیری و حافظه فضایی استفاده شد [16]. این دستگاه Y شکل دارای سه بازوی کاملاً مشابه به ابعاد 5/17×60 سانتیمتر و ارتفاع 30 سانتیمتر و از جنس شیشه شفاف است. میلههای آبکاری کروم نیکل در کف هر شاخه به فواصل یک سانتیمتر از هم به دو طرف دیوار متصل شده است.
احساس ناخوشایند (شوک الکتریکی) از طریق این میلهها به حیوان منتقل میشود. انتهای هر بازو دارای یک منبع نوری (لامپ 12 ولت) است. سطح بالای دستگاه نیز توسط سرپوشهای کشویی مسدود شده است تا از خروج حیوان در حین آموزش جلوگیری شود. در قسمت کنترل دستگاه مشخصات تحریک نظیر طول تحریک، فرکانس تحریک، فاصله زمانی بین روشنشدن لامپ و اعمال تحریک، فاصله زمانی بعد از عمل تحریک و شمارش تعداد دفعات تحریک قابل تنظیم است. دستگاه باید در یک محیط تاریک، آرام و بیسروصدا قرار گیرد.
روز اول آموزش به مدت 15 دقیقه به حیوان اجازه داده میشود تا با شکل ظاهری ماز آشنا شود. سپس از بازویی که حیوان در آن قرار دارد آموزش آغاز میشود. بازوها بر اساس جدول تصادفی انتخاب و با فشاردادن یک دکمه روی دستگاه کنترلی، چراغ یکی از بازوهای ماز روشن میشود. در یک فاصله زمانی کوتاه (پنج ثانیه) موش فرصت دارد تا از محل تاریک خارج و وارد بازوی روشن شود؛ در این صورت ورود موش به بازوی روشن به عنوان انتخاب صحیح محسوب میشود، در غیر این صورت بعد از پنج ثانیه شوک الکتریکی به پاهای موش وارد شده، که در این صورت ورود موش به بازوی روشن را به عنوان انتخاب صحیح و ورود به بازوی تاریک را به عنوان انتخاب غلط در نظر گرفتیم.
بر اساس جدول تصادفی به هر موش در هر روز 30 بار آموزش داده شد و در پایان هر جلسه تعداد پاسخهای صحیح محاسبه شد. جلسات آموزش به مدت پنج روز متوالی ادامه مییابد تا موشها به معیار پاسخ صحیح برسند؛ یعنی از 30 بار آموزش در روز حداقل 26 انتخاب صحیح داشته باشند. آزمون فراخوانی حافظه 25 روز بعد از آموزش به منظور ارزیابی حافظه بلندمدت انجام گرفت. در این آزمون حافظه هرکدام از حیوانات در روز سیام به صورت یک جلسه مورد ارزیابی قرار گرفت و مقایسه نتایج آن با نتایج روز پنجم آموزش انجام شد [16].
نتایج حاصل از این پژوهش به صورت توصیفی و تحلیلی با استفاده از آزمونهای آماری پارامتریک با نرم افزار SPSS بررسی شدند. به منظور مقایسه میانگین تعداد پاسخ صحیح در گروههای مختلف و تعیین اینکه آیا گروهها با یکدیگر اختلاف دارند یا نه، از آنالیز واریانس با اندازهگیری تکراری و آزمون تکمیلی TUKEY استفاده شد. مقایسه گروههای مختلف در پنج روز متوالی آموزش با روش آماری آنالیز واریانس یکطرفه و آزمون تکمیلی TUKEY انجام شد. به منظور مقایسه میانگین پاسخ صحیح روز پنجم و آزمون حافظه روز سیام از آزمون تی زوجی استفاده شد. در این بررسی 0/05˂P به عنوان سطح معنیداری در نظر گرفته شد.
یافتهها
در این مطالعه نتایج حاصل از آنالیز واریانس با اندازهگیری تکراری نشان داد که گروه، زمان و اثر متقابل گروه و زمان، تأثیر معنیداری بر یادگیری فضایی دارد (0/001˂P). در مقایسه گروههای مختلف در پنج روز متوالی آموزش با روش آنالیز واریانس یکطرفه نشان داده شد که میزان یادگیری فضایی بین گروه کنترل و شاهد تخریب در هیچکدام از روزها دارای تفاوت معنیدار نبود. از طرف دیگر میزان یادگیری فضایی بین گروههای کنترل و تخریب در روزهای اول، دوم، سوم، چهارم و پنجم (0/001˂P) دارای تفاوت معنیدار بود. همچنین در این گروهها بین میانگین پاسخ صحیح روز پنجم آموزش و آزمون فراخوانی حافظه روز سیام اختلاف معنیداری وجود نداشت (تصویر شماره 1).
بیماری آلزایمر شایعترین شکل دمانس است که به واسطه رسوبات خارج سلولی پلاکهای آمیلوئید بتا و تجمعات داخل سلولی کلافههای نروفیبریلاری که از عوامل سمیت عصبی و فقدان سیناپسی هستند منجر به نورودژنراسیون میشود [1]. علاوه بر این، اختلال در نورونهای کولینرژیک یا گیرندههای پس سیناپسی استیل کولین، مستقیماً با نقص شناختی ایجادشده در بیماری آلزایمر در ارتباط هستند. نشان داده شده است که استیل کولین و سیگنالینگ کولینرژیک جهت اعمال شناختی از جمله یادگیری و حافظه ضروری هستند [2]. اختلال در عملکرد و یا فقدان گروههای سلولی کولینرژیک در قاعده مغز جلویی از جمله هستههای قاعدهای مگنوسلولاریس در جوندگان و یا معادل آن هستههای قاعدهای مینرت در انسان از اولین وقایع پاتولوژیک در پاتوژنز بیماری آلزایمر هستند [3].
ممانتین آنتاگونیست غیررقابتی، گیرنده NMDA است که به صورت بالینی جهت درمان بیماری آلزایمر مورد استفاده قرار میگیرد. تحقیقات پیشین تأثیر ممانتین را بر افزایش سطوح خارج سلولی استیل کولین در هسته اکومبنس، نواحی تگمنتال شکمی [4] و هیپوکامپ [5] و همچنین بهبود نقص حافظه فضایی در موشهای مدل ترانسژنیک بیماری آلزایمر نشان دادهاند [6]. علاوه براین نشان داده شده است که درمان مزمن ممانتین به مدت 28 روز با کاهش آستروگلیوزیس، افزایش غلظتهای BDNF و GDNF، موجب محافظت عصبی، کاهش حجم آسیب و کاهش آتروفی مغزی ثانویه میشود [7].
برخی شواهد نقش مواد غذایی را در پیشگیری و یا کاهش ریسک ابتلا به بیماری آلزایمر نشان میدهند. با توجه به اینکه التهاب و آسیب اکسیداتیو نورونها میتواند عامل مرگ نورونها در بیماری آلزایمر باشد، احتمالاً مواد غذایی با ویژگیهای ضدالتهابی یا آنتیاکسیدانی خود نقش مهمی در کاهش ابتلا و مهار پیشرفت زوال عقل دارند [8]. برخی شواهد تأثیر ویتامین D را به عنوان یک عامل ضدالتهابی نشان دادهاند [9] که سرکوب سایتوکینهای پیشالتهابی در مغز احتمالاً مکانیسمی برای اعمال محافظت عصبی به وسیله ی ویتامین D است [10]. همچنین نشان داده شده است که ویتامین D در بیماران مبتلا به آلزایمر موجب تحریک فاگوسیتوز Aβ در ماکروفاژهای نوع I و II، بازجذب و کلیرانس Aβ میشود [11]. علاوه بر این، تأثیر ویتامین D بر افزایش آزادسازی فاکتور رشد عصب در نورونهای هیپوکامپ موشهای صحرایی نیز نشان داده شده است [12].
با توجه به تأثیر ممانتین در افزایش غلظت سیناپسی استیل کولین و نقش آن در محافظت عصبی و همچنین با در نظر گرفتن تأثیر ویتامین D در افزایش آزادسازی NGF، سرکوب سایتوکینهای پیشالتهابی و نیز اثرات آنتیاکسیدانی آن، در مطالعه حاضر بر آن شدیم تا پس از القای مدل آلزایمر از طریق تخریب الکتریکی دوطرفه NBM اثرات همافزایی ممانتین و ویتامین D را بر بهبود اختلالات یادگیری و حافظه فضایی مورد بررسی قرار دهیم.
مواد و روشها
در این مطالعه تجربی از موشهای صحرایی نر بالغ از نژاد ویستار با محدوده وزنی 20±200 گرم استفاده شد. موشها در گروههای چهارتایی در هر قفس، در خانه حیوانات با درجه حرارت کنترلشده (24-20 درجه سانتیگراد) و تحت چرخه روشنایی تاریکی 12ساعته نگهداری شدند و آب و غذا به مقدار کافی در دسترس داشتند. آزمایشات رفتاری در دوره روشنایی و با استفاده از دستگاه ماز Y شکل انجام گرفت. مواد مورد استفاده ممانتین، ویتامین D و روغن کنجد بودند که از شرکت سیگما تهیه شدند. در روز آزمایش غلظتهای مورد نظر ممانتین و ویتامین D به ترتیب توسط حلال سالین 0/9 درصد و روغن کنجد به صورت روزانه آماده میشد. موشها به طور تصادفی به 9 گروه (7=n) تقسیم شدند.
گروه کنترل: گروهی که تحت هیچگونه تزریق یا جراحی قرار نگرفتند. گروه ضایعهدیده (آلزایمری): گروهی که در آنها تحت عمل جراحی استرئوتاکسیک الکترود تخریب به صورت دوطرفه وارد NBM شد و با عبور جریان الکتریکی عمل تخریب انجام شد. گروه شاهد تخریب: گروهی که تحت جراحی و ورود الکترود به NBM بدون تخریب این هسته قرار گرفتند. گروه تخریب + روغن کنجد: گروهی که تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند و روغن کنجد (حلال ویتامین D) را به میزان 0/2 میلیلیتر به مدت 10 روز با شروع سه روز قبل از تخریب NBM به صورت تزریق داخل صفاقی دریافت کردند. گروه تخریب + سالین: گروهی که تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند و یک هفته بعد، سالین (حلال ممانتین) را به میزان 0/2 میلیلیتر به مدت پنج روز نیمساعت قبل از آموزش به صورت تزریق داخل صفاقی دریافت کردند. گروه تخریب + روغن کنجد + سالین: گروهی که تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند. این گروه روغن کنجد (حلال ویتامین D) را به مدت 10 روز با شروع سه روز قبل از تخریب و سالین (حلال ممانتین) را به میزان 0/2 میلیلیتر به مدت پنج روز نیمساعت قبل از آموزش به صورت تزریق داخل صفاقی دریافت کردند.
گروه تخریب+ ویتامین D: این گروه تحت عمل جراحی تخریب الکتریکی دو طرفه ی NBM قرار گرفتند و یک هفته بعد پنج میکروگرم بر کیلوگرم ویتامین D را به مدت 10 روز با شروع 3 روز قبل از تخریب به صورت تزریق داخل صفاقی دریافت کردند [13]. گروه تخریب + ممانتین: این گروه تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند و یک هفته بعد سه میلیگرم بر کیلوگرم ممانتین را به مدت پنج روز نیمساعت قبل از آموزش به صورت تزریق داخلصفاقی دریافت کردند [14]. تخریب + ویتامینD + ممانتین: گروهی که تحت عمل جراحی تخریب الکتریکی دوطرفه NBM قرار گرفتند. این گروه پنج میکروگرم بر کیلوگرم ویتامین D را به مدت 10 روز با شروع سه روز قبل از تخریب و سه میلیگرم بر کیلوگرم ممانتین را به مدت پنج روز نیمساعت قبل از آموزش به صورت تزریق داخل صفاقی دریافت کردند. گروه کنترل و سایر گروهها یک هفته بعد از جراحی (دوره بهبودی) به مدت پنج روز در دستگاه ماز Y شکل آموزش دیدند.
موشها جهت تخریب الکتریکی هسته NBM تحت بیهوشی عمومی با تزریق داخل صفاقی مخلوطی متشکل از 78 میلیگرم بر کیلوگرم کلروهیدرات کتامین 10 درصد و سه میلیگرم بر کیلوگرم زایلازین دو درصد قرار گرفتند [15] و سپس در دستگاه استرئوتاکسی (Stoelting, USA) ثابت شدند. میله دندانی 3/3 میلیمتر زیر صفر افقی قرار گرفت تا مطابق اطلس، وضعیت مناسب جمجمه حاصل شود. سپس موهای پشت سر حیوان از ناحیه بین چشمها تا گوشها تراشیده و پوست این ناحیه ضدعفونی شد. با کمک اسکالپل یک برش طولی در پوست ناحیه پشت سر حیوان داده شد و بعد از کنارزدن بافتهای پیوندی، محل موردنظر با نرمال سالین تمیز شد تا درزهای جمجمه نمایان شوند. مختصات مورد استفاده برای NBM طبق اطلس پاکسینوس و واتسون عبارت بود از: 3/1AP=- از برگما، 8/2ML=± از خط وسط و 6/7DV=- از سطح سخت شامه.
با استفاده از دستگاه ایجادکننده ضایعه (Lesion Making Device, UGO Basile) پس از قرارگرفتن الکترود در نقطه مورد نظر با عبور جریان الکتریکی مستقیم با شدت 5/0 میلیآمپر به مدت سه ثانیه [15] NBM در هر دو نیمکره مغزی به صورت الکتریکی تخریب شد و مدل آلزایمر ایجاد شد.
جهت بررسی روند یادگیری و حافظه در مدلهای آزمایشگاهی از دو روش تنبیه (دریافت شوک یا احساس ناخوشایند) و تشویق (دریافت پاداش مثل آب و غذا) استفاده میشود که با توجه به تداخل احتمالی برخی داروها در مکانیسم اشتها، به نظر میرسد برای بررسی تأثیر داروها بر روند یادگیری، روش تنبیه مناسبتر است. با توجه به اینکه هیپوکامپ در حافظه فضایی نقش عمدهای دارد در این تحقیق از دستگاه ماز Y شکل به منظور بررسی یادگیری و حافظه فضایی استفاده شد [16]. این دستگاه Y شکل دارای سه بازوی کاملاً مشابه به ابعاد 5/17×60 سانتیمتر و ارتفاع 30 سانتیمتر و از جنس شیشه شفاف است. میلههای آبکاری کروم نیکل در کف هر شاخه به فواصل یک سانتیمتر از هم به دو طرف دیوار متصل شده است.
احساس ناخوشایند (شوک الکتریکی) از طریق این میلهها به حیوان منتقل میشود. انتهای هر بازو دارای یک منبع نوری (لامپ 12 ولت) است. سطح بالای دستگاه نیز توسط سرپوشهای کشویی مسدود شده است تا از خروج حیوان در حین آموزش جلوگیری شود. در قسمت کنترل دستگاه مشخصات تحریک نظیر طول تحریک، فرکانس تحریک، فاصله زمانی بین روشنشدن لامپ و اعمال تحریک، فاصله زمانی بعد از عمل تحریک و شمارش تعداد دفعات تحریک قابل تنظیم است. دستگاه باید در یک محیط تاریک، آرام و بیسروصدا قرار گیرد.
روز اول آموزش به مدت 15 دقیقه به حیوان اجازه داده میشود تا با شکل ظاهری ماز آشنا شود. سپس از بازویی که حیوان در آن قرار دارد آموزش آغاز میشود. بازوها بر اساس جدول تصادفی انتخاب و با فشاردادن یک دکمه روی دستگاه کنترلی، چراغ یکی از بازوهای ماز روشن میشود. در یک فاصله زمانی کوتاه (پنج ثانیه) موش فرصت دارد تا از محل تاریک خارج و وارد بازوی روشن شود؛ در این صورت ورود موش به بازوی روشن به عنوان انتخاب صحیح محسوب میشود، در غیر این صورت بعد از پنج ثانیه شوک الکتریکی به پاهای موش وارد شده، که در این صورت ورود موش به بازوی روشن را به عنوان انتخاب صحیح و ورود به بازوی تاریک را به عنوان انتخاب غلط در نظر گرفتیم.
بر اساس جدول تصادفی به هر موش در هر روز 30 بار آموزش داده شد و در پایان هر جلسه تعداد پاسخهای صحیح محاسبه شد. جلسات آموزش به مدت پنج روز متوالی ادامه مییابد تا موشها به معیار پاسخ صحیح برسند؛ یعنی از 30 بار آموزش در روز حداقل 26 انتخاب صحیح داشته باشند. آزمون فراخوانی حافظه 25 روز بعد از آموزش به منظور ارزیابی حافظه بلندمدت انجام گرفت. در این آزمون حافظه هرکدام از حیوانات در روز سیام به صورت یک جلسه مورد ارزیابی قرار گرفت و مقایسه نتایج آن با نتایج روز پنجم آموزش انجام شد [16].
نتایج حاصل از این پژوهش به صورت توصیفی و تحلیلی با استفاده از آزمونهای آماری پارامتریک با نرم افزار SPSS بررسی شدند. به منظور مقایسه میانگین تعداد پاسخ صحیح در گروههای مختلف و تعیین اینکه آیا گروهها با یکدیگر اختلاف دارند یا نه، از آنالیز واریانس با اندازهگیری تکراری و آزمون تکمیلی TUKEY استفاده شد. مقایسه گروههای مختلف در پنج روز متوالی آموزش با روش آماری آنالیز واریانس یکطرفه و آزمون تکمیلی TUKEY انجام شد. به منظور مقایسه میانگین پاسخ صحیح روز پنجم و آزمون حافظه روز سیام از آزمون تی زوجی استفاده شد. در این بررسی 0/05˂P به عنوان سطح معنیداری در نظر گرفته شد.
یافتهها
در این مطالعه نتایج حاصل از آنالیز واریانس با اندازهگیری تکراری نشان داد که گروه، زمان و اثر متقابل گروه و زمان، تأثیر معنیداری بر یادگیری فضایی دارد (0/001˂P). در مقایسه گروههای مختلف در پنج روز متوالی آموزش با روش آنالیز واریانس یکطرفه نشان داده شد که میزان یادگیری فضایی بین گروه کنترل و شاهد تخریب در هیچکدام از روزها دارای تفاوت معنیدار نبود. از طرف دیگر میزان یادگیری فضایی بین گروههای کنترل و تخریب در روزهای اول، دوم، سوم، چهارم و پنجم (0/001˂P) دارای تفاوت معنیدار بود. همچنین در این گروهها بین میانگین پاسخ صحیح روز پنجم آموزش و آزمون فراخوانی حافظه روز سیام اختلاف معنیداری وجود نداشت (تصویر شماره 1).
در بررسی اثر حلال ویتامین D (روغن کنجد)، حلال ممانتین (سالین) و تأثیر توأم آنها نتایج آنالیز آماری نشان داد که میانگین تعداد پاسخ صحیح بین گروه تخریب با گروههای تخریب + روغن کنجد، تخریب + سالین و تخریب + روغن کنجد + سالین در هیچکدام از روزها تفاوت معنیداری را نشان نمیدهند. علاوه بر این، بین میانگین تعداد پاسخ صحیح روز پنجم آموزش و آزمون فراخوانی حافظه روز سیام در هرگروه اختلاف معنیداری وجود نداشت (تصویر شماره 2).
در بررسی اثرات ویتامین D، ممانتین و تأثیر توأم آنها بر یادگیری و حافظه فضایی نتایج آنالیز آماری نشاندهنده افزایش میانگین تعداد پاسخ صحیح در روزهای اول (0/05˂P)، دوم (0/05˂P)، سوم (0/01˂P)، چهارم (0/05˂P) و پنجم (0/05˂P) آموزش در گروه تخریب + ویتامین D، در روزهای دوم (0/05˂P)، سوم (0/05˂P) و چهارم (0/05˂P) آموزش در گروه تخریب + ممانتین و در روزهای اول (0/01˂P)، دوم (0/001˂P)، سوم (0/001˂P)، چهارم (0/01˂P) و پنجم (0/05˂P) آموزش در گروه تخریب + ویتامین D + ممانتین در مقایسه با گروه تخریب است که نتایج این بررسی نشاندهنده اثرات افزایشی تأثیر توأم ویتامین D و ممانتین بر میانگین تعداد پاسخ صحیح در روزهای اول، دوم، سوم و چهارم آموزش است. علاوه بر این در گروههای مورد بررسی بین میانگین تعداد پاسخ صحیح در روز پنجم آموزش با آزمون فراخوانی حافظه در روز سیام اختلاف معنیداری مشاهده نشد (تصویر شماره 3).
بحث
با توجه به اینکه اثرات ممانتین و ویتامین D بهتنهایی در درمان اختلالات شناختی در بیماران مبتلا به آلزایمر ناکافی است که این امر در یافتههای این پژوهش نیز نشان داده شده است در مطالعه حاضر امکان افزایش اثربخشی مقادیر درمانی ممانتین تحت تأثیر ویتامین D بررسی شده است. بدین منظور مقادیر با تأثیر کم این دو ماده انتخاب و تأثیر توأم آنها بر یادگیری و حافظه فضایی در گروههای با تخریب الکتریکی دوطرفه NBM مورد بررسی قرار گرفت. یافتههای این مطالعه نشان میدهند که درمان توأم ویتامین D و ممانتین از طریق تزریق داخل صفاقی ویتامین D به مدت 10 روز با شروع سه روز قبل از تخریب NBM و القای مدل بیماری آلزایمر و تزریق داخل صفاقی ممانتین به مدت پنج روز با شروع هفت روز پس از تخریب NBM نسبت به تجویز هریک از این دو بهتنهایی دارای تأثیر بیشتری در بهبود اختلال یادگیری و حافظه فضایی در موشهای مدل بیماری آلزایمر است. NBM از هستههای کولینرژیک قاعده مغز جلویی است [3] که در مطالعه حاضر تخریب الکتریکی دوطرفه آن منجر به کاهش معنیدار فرایند یادگیری و حافظه فضایی شد (تصویر شماره 1). در همین راستا ژائو و همکاران نیز نشان دادهاند که تخریب NBM به وسیله ایبوتنیک اسید منجر به اختلال حافظه در آزمون ماز آبی موریس و کاهش فعالیت کولین استیل ترانسفراز (ChAT) در قشر فرونتال و هیپوکامپ میشود [17]. علاوه بر این نشان داده شده است که تخریب دوطرفه NBM به وسیله ایبوتنیک اسید منجر به کاهش سطوح استیل کولین، کولین استراز و کولین استیل ترانسفراز در قشر مغز و اختلال حافظه فضایی در آزمون ماز آبی موریس و حافظه شناختی در آزمون شناخت اشیای جدید میشود [18] که این نتایج همراستا با نتایج این پژوهش هستند.
در این بررسی اختلاف معنیداری در یادگیری فضایی موشهای صحرایی در گروههای کنترل و شاهد تخریب مشاهده نشد که نشان میدهد مراحل مختلف بیهوشی، جراحی و ورود الکترود به NBM بدون ایجاد تخریب اثری بر یادگیری فضایی در موشهای صحرایی ندارد (تصویر شماره 1). همچنین مقایسه نتایج بین گروههای تخریب، تخریب + روغن کنجد، تخریب + سالین و تخریب + روغن کنجد + سالین نشان داد که روغن کنجد (حلال ویتامین D)، سالین (حلال ممانتین) و تجویز توأم آنها هیچگونه تأثیری بر یادگیری فضایی ندارد (تصویر شماره 2).
علاوه بر این یافتههای این مطالعه نشان میدهد که ویتامین D و ممانتین در تجویز توأم دارای اثرات همافزایی بر بهبود یادگیری فضایی در موشهای صحرایی با تخریب الکتریکی دوطرفه NBM هستند (تصویر شماره 3). مقادیر ویتامین D و ممانتین بر اساس مطالعات انجامشده پیشین انتخاب شدند [14 ،13]. در همین راستا در مطالعات چن و همکاران نیز نشان داده شده است که در موشهای ترانسژنیک مدل آلزایمر اسیدفولیک موجب افزایش اثرات ممانتین در محافظت عصبی نورونهای ناحیه CA1 هیپوکامپ و یادگیری فضایی در ماز آبی موریس میشود [19].
در مطالعات احمدی زهرانی و همکاران نیز تأثیر ممانتین در بهبود نقایص شناختی اختلالات خاص یادگیری که یک اختلال عصبی رشدی است نشان داده شد [20]. از طرف دیگر در مطالعات دی و همکاران نشان داده شد که 17-β- استرادیول نیز که همانند ویتامین D دارای اثرات محافظت عصبی است در درمان توأم با ممانتین در مدل آسیب مغزی تروماتیک منجر به کاهش دژنراسیون نورونی و افزایش بقاء نورونها میشود [21]. نتایج مطالعات آنوایلر و همکاران در شرایط in vitro نیز نشاندهنده مهار دژنراسیون آکسونی القاشده به وسیله گلوتامات و Aβ در نورونهای قشری موشهای صحرایی تحت درمان توأم ممانتین و ویتامین D هستند [22] که با توجه به نتایج این مطالعه میتوان نتیجه گرفت که درمان توأم ممانتین و ویتامین D مؤثرتر از تجویز هریک از این دو ماده بهتنهایی است.
مکانیسم برهمکنش ممانتین و ویتامین D در مدل بیماری آلزایمر از طریق تخریب NBM تاکنون مورد بررسی قرار نگرفته است، اما مطالعات متعددی در خصوص مکانیسمهای عمل هریک از این دو بهتنهایی انجام شده است. به عنوان مثال نتایج یک مطالعه نشاندهنده اثرات ممانتین بر افزایش سطوح استیل کولین خارج سلولی در هیپوکامپ هستند [23]. همچنین در مطالعات اهالاینن روی موشهای صحرایی با تخریب فیمبریافورنیکس افزایش ناچیز سطوح استیل کولین نئوکورتکس و هیپوکامپ تحت درمان مزمن ممانتین و افزایش معنیدار آن تحت درمان حاد با ممانتین نشان داده شده است که با توجه به اینکه درمان مزمن ممانتین در بررسیهای رفتاری نسبت به درمان حاد آن دارای تأثیر بیشتری بر بهبود یادگیری و حافظه است، به نظر میرسد که اثرات درمانی ممانتین بر بهبود حافظه طولانیمدت دارای مکانیسمهای متفاوتی نسبت به اثرات درمانی آن بر بهبود حافظه کوتاهمدت افزایش سطوح استیل کولین در قشر و هیپوکامپ است [5]. علاوه بر این نشان داده شده است که ممانتین در غلظتهای درمانی موجب محافظت در برابر آسیب نورونی و آپوپتوز القاشده به وسیله تزریق مستقیم Aβ1-40 به هیپوکامپ میشود [24]. علاوه بر این، تأثیر ممانتین بر کاهش سطوح TNF-α در هیپوکامپ و کاهش سطوح IL-1β در قشر و هیپوکامپ در مدل آلزایمر القاشده به وسیله تزریق داخل هیپوکامپی Aβ نیز نشان داده شده است [25]. نتایج حاصل از مطالعه ما نیز از نظر تأثیر ممانتین بر بهبود یادگیری و حافظه با موارد پیشگفته همخوانی داشت.
از طرف دیگر بهبود نوروژنز و اعمال شناختی در موشهای ترانسژنیک مدل آلزایمر تحت درمان با مکمل ویتامین D نیز نشان داده شده است [26]. در مطالعات یامینی و همکاران نشان داده شد که پیش درمان با ویتامین D به طور مؤثری موجب بهبود حافظه فضایی در ماز آبی موریس میشود. علاوه بر این در این مطالعه کاهش استرس اکسیداتیو و افزایش سطوح استیل کولین استراز در کورتکس مغز و هیپوکامپ موشهای صحرایی مدل آلزایمر نیز تحت پیش درمان با ویتامین D بهبود یافت [27].
در بررسیهای پیوش و همکاران نیز مکمل ویتامین D3 موجب بازگشت تغییرات ایجادشده در گیرندههای کولینرژیک و فعالیت استیل کولین استراز در موشهای صحرایی دیابتیشده توسط STZ شد [28]. علاوه بر این، استفاده از مکمل ویتامین D در افراد میانسال مبتلا به کمبود این ویتامین، منجر به افزایش سطوح پلاسمایی Aβ40 شد که این نتایج نشاندهنده تأثیر ویتامین D بر کاهش Aβ در بافت مغزی [29] از طریق تحریک فاگوسیتوز Aβ توسط ماکروفاژهای نوع I و II، بازجذب و کلیرانس Aβ هستند [11].
در همن راستا در مطالعات بریونز و درویش در سال 2012 کاهش Aβ تحت تأثیر درمان با ویتامین D در موشهای صحرایی مسن نشان داده شد [30]. همچنین برخی مطالعات اثرات ضدالتهابی ویتامین D و تأثیر آن را بر بازگشت تغییرات التهابی مرتبط با سن در هیپوکامپ موشهای صحرایی نشان میدهند که در این زمینه سرکوب سایتوکینهای پیشالتهابی در مغز را میتوان به عنوان مکانیسمی برای اعمال محافظت عصبی ویتامین D در نظر گرفت [10 ،9]. بنابراین به نظر میرسد که در درمان توأم ممانتین و ویتامین D، ویتامین D با بهبود نوروژنز و اعمال شناختی، افزایش محافظت عصبی، کاهش التهاب و تنظیم اعمال کولینرژیک موجب بهبود حافظه و یادگیری در موشهای صحرایی مدل آلزایمر و تحت تیمار با ممانتین میشود.
نتیجهگیری
در این مطالعه از تخریب الکتریکی دوطرفه NBM به عنوان مدلی جهت القای بیماری آلزایمر در موشهای صحرایی استفاده شده است. با توجه به نتایج این پژوهش، تجویز توأم ویتامینD و ممانتین در مقادیر کم نسبت به تجویز هریک از این دو بهتنهایی دارای تأثیر بیشتری بر بهبود یادگیری و حافظه فضایی در موشهای مدل آلزایمر است.
پیشنهاد میشود که برای مطالعات بیشتر در این زمینه اثرات تجویز توأم ممانتین و ویتامین D بر سطوح پلاسمایی Aβ و همچنین استرس اکسیداتیو و فعالیت استیل کولین استراز در بافت مغزی موشهای صحرایی مدل آلزایمر بررسی شود.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این مطالعه با کد اخلاق EE/ 97, 24, 3061243/scu.ac.irتوسط کمیته اخلاق پژوهشی دانشگاه شهید چمران اهواز به تصویب رسیده است.
حامی مالی
این مقاله از حمایت مالی دانشگاه شهید چمران اهواز برخوردار بوده است
مشارکت نویسندگان
تمامی نویسندگان در نگارش این مقاله به یک اندازه مشارکت داشتهاند.
تعارض منافع
نویسندگان اعلام میدارند که هیچگونه تضاد منافعی در پژوهش حاضر وجود ندارد.
تشکر و قدردانی
بدینوسیله نویسندگان مراتب تشکر و قدردانی خود را از معاونت پژوهشی دانشگاه شهید چمران اهواز به جهت همکاری و مساعدت در انجام این پروژه علمی- پژوهشی اعلام می دارند.
References
Agatonovic-Kustrin S, Kettle C, Morton DW. A molecular approach in drug development for Alzheimer’s disease. Biomed Pharmacother 2018; 106:553-65. [DOI:10.1016/j.biopha.2018.06.147] [PMID]
Zhao LX, Ge YH, Xiong CH, Tang L, Yan YH, Law PY, et al. M1 muscarinic receptor facilitates cognitive function by interplay with AMPA receptor GluA1 subunit. FASEB J. 2018; 32(8):4247-57. [DOI:10.1096/fj.201800029R] [PMID]
Nyakas C, Granic I, Halmy LG, Banerjee P, Luiten PG. The basal forebrain cholinergic system in aging and dementia. Rescuing cholinergic neurons from neurotoxic amyloid-β42 with memantine. Behav Brain Res. 2011; 221(2):594-603. [DOI:10.1016/j.bbr.2010.05.033] [PMID]
Shearman E, Rossi S, Szasz B, Juranyi Z, Fallon S, Pomara N, et al. Changes in cerebral neurotransmitters and metabolites induced by acute donepezil and memantine administrations: a microdialysis study. Brain Res Bull. 2006; 69(2):204-13. [DOI:10.1016/j.brainresbull.2005.12.001] [PMID]
Ihalainen J, Sarajärvi T, Rasmusson D, Kemppainen S, Keski-Rahkonen P, Lehtonen M, et al. Effects of memantine and donepezil on cortical and hippocampal acetylcholine levels and object recognition memory in rats. Neuropharmacology. 2011; 61(5-6):891-99. [DOI:10.1016/j.neuropharm.2011.06.008] [PMID]
Nagakura A, Shitaka Y, Yarimizu J, Matsuoka N. Characterization of cognitive deficits in a transgenic mouse model of Alzheimer’s disease and effects of donepezil and memantine. Eur J Pharmacol. 2013; 703(1-3):53-61. [DOI:10.1016/j.ejphar.2012.12.023] [PMID]
Wang YC, Sanchez-Mendoza EH, Doeppner TR, Hermann DM. Post-acute delivery of memantine promotes post-ischemic neurological recovery, peri-infarct tissue remodeling, and contralesional brain plasticity. J Cereb Blood Flow Metab. 2017; 37(3):980-93. [DOI:10.1177/0271678X16648971] [PMID] [PMCID]
Taghizadeh M, Djazayery A, Salami M, Eshraghian MR, Zavareh SA. Vitamin-D-free regimen intensifies the spatial learning deficit in Alzheimer’s disease. Int J Neurosci. 2011; 121(1):16-24. [DOI:10.3109/00207454.2010.523132] [PMID]
Moore ME, Piazza A, McCartney Y, Lynch MA. Evidence that vitamin D3 reverses age-related inflammatory changes in the rat hippocampus. Biochem Soc Trans. 2005; 33(Pt 4):573-77. [DOI:10.1042/BST0330573] [PMID]
Banerjee A, Khemka VK, Ganguly A, Roy D, Ganguly U, Chakrabarti S. Vitamin D and Alzheimer’s Disease: Neurocognition to Therapeutics. Int J Alzheimers Dis. 2015; 2015:192747. [DOI:10.1155/2015/192747] [PMID] [PMCID]
Masoumi A, Goldenson B, Ghirmai S, Avagyan H, Zaghi J, Abel K, et al. 1alpha,25-dihydroxyvitamin D3 interacts with curcuminoids to stimulate amyloid-beta clearance by macrophages of Alzheimer’s disease patients. J Alzheimers Dis. 2009; 17(3):703-17. [DOI:10.3233/JAD-2009-1080] [PMID]
Gezen-Ak D, Dursun E, Yilmazer S. The Effect of Vitamin D Treatment On Nerve Growth Factor (NGF) Release From Hippocampal Neurons. Noro Psikiyatr Ars. 2014; 51(2):157-62. [DOI:10.4274/npa.y7076] [PMID] [PMCID]
Mashayekhi F, salehi Z, Mirzajani E. [Effects of vitamin D on myelin basic protein expression in corpus callosum of mouse model of experimental autoimmune encephalomyelitis induced by Cuprizone (Persian)]. Journal of Cell & Tissue. 2018; 8(4):314-21.
Zamani N, Moazedi AA, Afarinesh Khaki MR, Pourmehdi Boroujeni M. [Effect of memantine on spatial learning andmemory in electrical leisions model of nucleus basalis magnocellularis: animal model of Alzheimer’s disease (Persian)]. J Gorgan Univ Med Sci 2018; 20(1):43-50.
Ashkavandi S, Moazedi AA, Semnanian S, Eshagh-Harooni H, Mohammadi T, Pourmehdi-Boroujeni M. The effect of methylprednisolone on spatial learning and memory in adult male rats using an experimental model of Alzheimer’s disease. Feyz, J Kashan Univ of Med Sci 2015; 19(2):102-10.
Hoveida R, Moazedi AA, Rasekh AR. [The effect of intra-Hippocampal CA1 area injection of Estradiol Benzoate on the spatial learning and memory in adult male rats (Persian)]. Modares J Med Sci. 2005; 7(2):115-24.
Zhao Z, Zhao S, Xu N, Yu C, Guan S, Liu X, et al. Lovastatin improves neurological outcome after nucleus basalis magnocellularis lesion in rats. Neuroscience. 2010; 167(3):954-63. [DOI:10.1016/j.neuroscience.2010.02.054] [PMID]
Hou XQ, Zhang L, Yang C, Rong CP, He WQ, Zhang CX, et al. Alleviating effects of Bushen-Yizhi formula on ibotenic acid-induced cholinergic impairments in rat. Rejuvenation Res. 2015; 18(2):111-27. [DOI:10.1089/rej.2014.1603] [PMID] [PMCID]
Chen TF, Huang RF, Lin SE, Lu JF, Tang MC, Chiu MJ. Folic Acid potentiates the effect of memantine on spatial learning and neuronal protection in an Alzheimer’s disease transgenic model. J Alzheimers Dis. 2010; 20(2):607-15. [DOI:10.3233/JAD-2010-1396] [PMID]
Ahmadi Zahrani E, Nokani M, Keypour M, Alaghemand A. [Effectiveness of memantine in improvement of cognitive deficits in specific learning disorder (Persian)]. Arak Med Univ J. 2016; 19(114):1-11.
Day NL, Carle MS, Floyd CL. Post-injury administration of a combination of memantine and 17β-estradiol is protective in a rat model of traumatic brain injury. Neurochem Int. 2017; 111:57-68. [DOI:10.1016/j.neuint.2017.04.018] [PMID]
Annweiler C, Brugg B, Peyrin JM, Bartha R, Beauchet O. Combination of memantine and vitamin D prevents axon degeneration induced by amyloid-beta and glutamate. Neurobiol Aging. 2014; 35(2):331-35. [DOI:10.1016/j.neurobiolaging.2013.07.029] [PMID]
Yamaguchi Y, Takeda K, Hino M. Combination effects of ZSET1446/ST101 with memantine on cognitive function and extracellular acetylcholine in the hippocampus. J Pharmacol Sci. 2013; 123(4):347-55. [DOI:10.1254/jphs.13042FP] [PMID]
Miguel-Hidalgo JJ, Alvarez XA, Cacabelos R, Quack G. Neuroprotection by memantine against neurodegeneration induced by beta-amyloid (1-40). Brain Res. 2002; 958(1):210-21. [DOI:10.1016/S0006-8993(02)03731-9]
Budni J, Feijó DP, Batista-Silva H, Garcez ML, Mina F, Belletini-Santos T, et al. Lithium and memantine improve spatial memory impairment and neuroinflammation induced by β-amyloid 1-42 oligomers in rats. Neurobiol Learn Mem. 2017; 141:84-92. [DOI:10.1016/j.nlm.2017.03.017] [PMID]
Morello M, Landel V, Lacassagne E, Baranger K, Annweiler C, Féron F, et al. Vitamin D Improves Neurogenesis and Cognition in a Mouse Model of Alzheimer’s Disease. Mol Neurobiol. 2018; 55(8):6463-79. [DOI:10.1007/s12035-017-0839-1] [PMID] [PMCID]
Yamini P, Ray RS, Chopra K. Vitamin D3 attenuates cognitive deficits and neuroinflammatory responses in ICV-STZ induced sporadic Alzheimer’s disease. Inflammopharmacology. 2018; 26(1):39-55. [DOI:10.1007/s10787-017-0372-x] [PMID]
Peeyush KT, Savitha B, Sherin A, Anju TR, Jes P, Paulose CS. Cholinergic, dopaminergic and insulin receptors gene expression in the cerebellum of streptozotocin-induced diabetic rats: functional regulation with Vitamin D3 supplementation. Pharmacol Biochem Behav. 2010; 95(2):216-22. [DOI:10.1016/j.pbb.2010.01.008] [PMID]
Miller BJ, Whisner CM, Johnston CS. Vitamin D Supplementation Appears to Increase Plasma Aβ40 in Vitamin D Insufficient Older Adults: A Pilot Randomized Controlled Trial. J Alzheimers Dis. 2016; 52(3):843-47. [DOI:10.3233/JAD-150901] [PMID]
Briones TL, Darwish H. Vitamin D mitigates age-related cognitive decline through the modulation of pro-inflammatory state and decrease in amyloid burden. J Neuroinflammation. 2012; 9:244. [DOI:10.1186/1742-2094-9-244] [PMID] [PMCID]
Agatonovic-Kustrin S, Kettle C, Morton DW. A molecular approach in drug development for Alzheimer’s disease. Biomed Pharmacother 2018; 106:553-65. [DOI:10.1016/j.biopha.2018.06.147] [PMID]
Zhao LX, Ge YH, Xiong CH, Tang L, Yan YH, Law PY, et al. M1 muscarinic receptor facilitates cognitive function by interplay with AMPA receptor GluA1 subunit. FASEB J. 2018; 32(8):4247-57. [DOI:10.1096/fj.201800029R] [PMID]
Nyakas C, Granic I, Halmy LG, Banerjee P, Luiten PG. The basal forebrain cholinergic system in aging and dementia. Rescuing cholinergic neurons from neurotoxic amyloid-β42 with memantine. Behav Brain Res. 2011; 221(2):594-603. [DOI:10.1016/j.bbr.2010.05.033] [PMID]
Shearman E, Rossi S, Szasz B, Juranyi Z, Fallon S, Pomara N, et al. Changes in cerebral neurotransmitters and metabolites induced by acute donepezil and memantine administrations: a microdialysis study. Brain Res Bull. 2006; 69(2):204-13. [DOI:10.1016/j.brainresbull.2005.12.001] [PMID]
Ihalainen J, Sarajärvi T, Rasmusson D, Kemppainen S, Keski-Rahkonen P, Lehtonen M, et al. Effects of memantine and donepezil on cortical and hippocampal acetylcholine levels and object recognition memory in rats. Neuropharmacology. 2011; 61(5-6):891-99. [DOI:10.1016/j.neuropharm.2011.06.008] [PMID]
Nagakura A, Shitaka Y, Yarimizu J, Matsuoka N. Characterization of cognitive deficits in a transgenic mouse model of Alzheimer’s disease and effects of donepezil and memantine. Eur J Pharmacol. 2013; 703(1-3):53-61. [DOI:10.1016/j.ejphar.2012.12.023] [PMID]
Wang YC, Sanchez-Mendoza EH, Doeppner TR, Hermann DM. Post-acute delivery of memantine promotes post-ischemic neurological recovery, peri-infarct tissue remodeling, and contralesional brain plasticity. J Cereb Blood Flow Metab. 2017; 37(3):980-93. [DOI:10.1177/0271678X16648971] [PMID] [PMCID]
Taghizadeh M, Djazayery A, Salami M, Eshraghian MR, Zavareh SA. Vitamin-D-free regimen intensifies the spatial learning deficit in Alzheimer’s disease. Int J Neurosci. 2011; 121(1):16-24. [DOI:10.3109/00207454.2010.523132] [PMID]
Moore ME, Piazza A, McCartney Y, Lynch MA. Evidence that vitamin D3 reverses age-related inflammatory changes in the rat hippocampus. Biochem Soc Trans. 2005; 33(Pt 4):573-77. [DOI:10.1042/BST0330573] [PMID]
Banerjee A, Khemka VK, Ganguly A, Roy D, Ganguly U, Chakrabarti S. Vitamin D and Alzheimer’s Disease: Neurocognition to Therapeutics. Int J Alzheimers Dis. 2015; 2015:192747. [DOI:10.1155/2015/192747] [PMID] [PMCID]
Masoumi A, Goldenson B, Ghirmai S, Avagyan H, Zaghi J, Abel K, et al. 1alpha,25-dihydroxyvitamin D3 interacts with curcuminoids to stimulate amyloid-beta clearance by macrophages of Alzheimer’s disease patients. J Alzheimers Dis. 2009; 17(3):703-17. [DOI:10.3233/JAD-2009-1080] [PMID]
Gezen-Ak D, Dursun E, Yilmazer S. The Effect of Vitamin D Treatment On Nerve Growth Factor (NGF) Release From Hippocampal Neurons. Noro Psikiyatr Ars. 2014; 51(2):157-62. [DOI:10.4274/npa.y7076] [PMID] [PMCID]
Mashayekhi F, salehi Z, Mirzajani E. [Effects of vitamin D on myelin basic protein expression in corpus callosum of mouse model of experimental autoimmune encephalomyelitis induced by Cuprizone (Persian)]. Journal of Cell & Tissue. 2018; 8(4):314-21.
Zamani N, Moazedi AA, Afarinesh Khaki MR, Pourmehdi Boroujeni M. [Effect of memantine on spatial learning andmemory in electrical leisions model of nucleus basalis magnocellularis: animal model of Alzheimer’s disease (Persian)]. J Gorgan Univ Med Sci 2018; 20(1):43-50.
Ashkavandi S, Moazedi AA, Semnanian S, Eshagh-Harooni H, Mohammadi T, Pourmehdi-Boroujeni M. The effect of methylprednisolone on spatial learning and memory in adult male rats using an experimental model of Alzheimer’s disease. Feyz, J Kashan Univ of Med Sci 2015; 19(2):102-10.
Hoveida R, Moazedi AA, Rasekh AR. [The effect of intra-Hippocampal CA1 area injection of Estradiol Benzoate on the spatial learning and memory in adult male rats (Persian)]. Modares J Med Sci. 2005; 7(2):115-24.
Zhao Z, Zhao S, Xu N, Yu C, Guan S, Liu X, et al. Lovastatin improves neurological outcome after nucleus basalis magnocellularis lesion in rats. Neuroscience. 2010; 167(3):954-63. [DOI:10.1016/j.neuroscience.2010.02.054] [PMID]
Hou XQ, Zhang L, Yang C, Rong CP, He WQ, Zhang CX, et al. Alleviating effects of Bushen-Yizhi formula on ibotenic acid-induced cholinergic impairments in rat. Rejuvenation Res. 2015; 18(2):111-27. [DOI:10.1089/rej.2014.1603] [PMID] [PMCID]
Chen TF, Huang RF, Lin SE, Lu JF, Tang MC, Chiu MJ. Folic Acid potentiates the effect of memantine on spatial learning and neuronal protection in an Alzheimer’s disease transgenic model. J Alzheimers Dis. 2010; 20(2):607-15. [DOI:10.3233/JAD-2010-1396] [PMID]
Ahmadi Zahrani E, Nokani M, Keypour M, Alaghemand A. [Effectiveness of memantine in improvement of cognitive deficits in specific learning disorder (Persian)]. Arak Med Univ J. 2016; 19(114):1-11.
Day NL, Carle MS, Floyd CL. Post-injury administration of a combination of memantine and 17β-estradiol is protective in a rat model of traumatic brain injury. Neurochem Int. 2017; 111:57-68. [DOI:10.1016/j.neuint.2017.04.018] [PMID]
Annweiler C, Brugg B, Peyrin JM, Bartha R, Beauchet O. Combination of memantine and vitamin D prevents axon degeneration induced by amyloid-beta and glutamate. Neurobiol Aging. 2014; 35(2):331-35. [DOI:10.1016/j.neurobiolaging.2013.07.029] [PMID]
Yamaguchi Y, Takeda K, Hino M. Combination effects of ZSET1446/ST101 with memantine on cognitive function and extracellular acetylcholine in the hippocampus. J Pharmacol Sci. 2013; 123(4):347-55. [DOI:10.1254/jphs.13042FP] [PMID]
Miguel-Hidalgo JJ, Alvarez XA, Cacabelos R, Quack G. Neuroprotection by memantine against neurodegeneration induced by beta-amyloid (1-40). Brain Res. 2002; 958(1):210-21. [DOI:10.1016/S0006-8993(02)03731-9]
Budni J, Feijó DP, Batista-Silva H, Garcez ML, Mina F, Belletini-Santos T, et al. Lithium and memantine improve spatial memory impairment and neuroinflammation induced by β-amyloid 1-42 oligomers in rats. Neurobiol Learn Mem. 2017; 141:84-92. [DOI:10.1016/j.nlm.2017.03.017] [PMID]
Morello M, Landel V, Lacassagne E, Baranger K, Annweiler C, Féron F, et al. Vitamin D Improves Neurogenesis and Cognition in a Mouse Model of Alzheimer’s Disease. Mol Neurobiol. 2018; 55(8):6463-79. [DOI:10.1007/s12035-017-0839-1] [PMID] [PMCID]
Yamini P, Ray RS, Chopra K. Vitamin D3 attenuates cognitive deficits and neuroinflammatory responses in ICV-STZ induced sporadic Alzheimer’s disease. Inflammopharmacology. 2018; 26(1):39-55. [DOI:10.1007/s10787-017-0372-x] [PMID]
Peeyush KT, Savitha B, Sherin A, Anju TR, Jes P, Paulose CS. Cholinergic, dopaminergic and insulin receptors gene expression in the cerebellum of streptozotocin-induced diabetic rats: functional regulation with Vitamin D3 supplementation. Pharmacol Biochem Behav. 2010; 95(2):216-22. [DOI:10.1016/j.pbb.2010.01.008] [PMID]
Miller BJ, Whisner CM, Johnston CS. Vitamin D Supplementation Appears to Increase Plasma Aβ40 in Vitamin D Insufficient Older Adults: A Pilot Randomized Controlled Trial. J Alzheimers Dis. 2016; 52(3):843-47. [DOI:10.3233/JAD-150901] [PMID]
Briones TL, Darwish H. Vitamin D mitigates age-related cognitive decline through the modulation of pro-inflammatory state and decrease in amyloid burden. J Neuroinflammation. 2012; 9:244. [DOI:10.1186/1742-2094-9-244] [PMID] [PMCID]
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |