دوره 25، شماره 3 - ( مرداد و شهریور 1401 )
جلد 25 شماره 3 صفحات 353-338 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Ghaedmohammadi S, Bahrulolum H, Ahmadian G. A Systemic Review on Bacillus Subtilis Spore Structure and Its Applications in the Development of Mucosal Vaccines and Adjuvants. J Arak Uni Med Sci 2022; 25 (3) :338-353
URL: http://jams.arakmu.ac.ir/article-1-7181-fa.html
URL: http://jams.arakmu.ac.ir/article-1-7181-fa.html
قائدمحمدی سمیرا، بحرالعلوم حورا، احمدیان غلامرضا. مروری بر ساختار اسپور باسیلوس سوبتیلیس و کاربردهای آن در توسعه واکسنهای مخاطی و ادجوانت. مجله دانشگاه علوم پزشكي اراك. 1401; 25 (3) :338-353
1- گروه زیستشناسی سلولی و مولکولی، دانشگاه شیراز، مرکز آموزش عالی استهبان، استهبان، ایران.
2- پژوهشکده زیست فناوری صنعت و محیط زیست، پژوهشگاه ملی مهندسی ژنتیک و زیست فناوری، تهران، ایران.
3- پژوهشکده زیست فناوری صنعت و محیط زیست، پژوهشگاه ملی مهندسی ژنتیک و زیست فناوری، تهران، ایران. ،ahmadian@nigeb.ac.ir
2- پژوهشکده زیست فناوری صنعت و محیط زیست، پژوهشگاه ملی مهندسی ژنتیک و زیست فناوری، تهران، ایران.
3- پژوهشکده زیست فناوری صنعت و محیط زیست، پژوهشگاه ملی مهندسی ژنتیک و زیست فناوری، تهران، ایران. ،
متن کامل [PDF 1651 kb]
(1450 دریافت)
| چکیده (HTML) (2326 مشاهده)
متن کامل: (3366 مشاهده)
مقدمه
نمایش سطحی یک تکنیک مولکولی است که توسط آن پپتیدها و پروتئینهای هترولوگ در سطح خارجی باکتریوفاژها، سلولها یا اسپورها تثبیت میشوند. این تکنیک در حال تبدیل شدن به یک ابزار تحقیقاتی در زمینههای مختلف میکروبیولوژی، زیستشناسی مولکولی، واکسنشناسی و بیوتکنولوژی است. این رویکرد مبتنی بر ایده استفاده از پروتئینهای سطحی طبیعی به عنوان لنگر برای هدفگیری پروتئینهای مورد نظر است که پروتئینهای مسافری نیز نامیده میشوند.
رایجترین رویکردها برای نمایش سطحی پروتئین شامل استفاده از سلولهای مخمر یا پروکاریوتی، فاژها و اسپورهای باکتریایی است. فناوری نمایش سطحی طیف وسیعی از کاربردهای بیوتکنولوژیکی و صنعتی را نشان داده است. از جمله این کاربردها شامل توسعه واکسنهای زنده، غربالگری کتابخانههای پپتیدی، تولید آنتیبادی، جاذبهای زیستی برای حذف مواد شیمیایی مضر و فلزات سنگین، بیوکاتالیستهای کل سلولی با بیحرکت کردن آنزیمها، توسعه حسگرهای زیستی و غیره هستند [1، 2].
اولین گزارشها درباره نمایش پروتئینهای هترولوگ روی سطح باکتریها در سال 1986 مطرح شد [3، 4]. پس از آن، سیستمهای نمایشی متنوع دیگری نیز روی سطح مخمر، باکتریهای گرم مثبت و باکتریهای گرم منفی گسترش یافت [5-7]. اولین سیستم بیان سطحی را جورج اسمیت در اواسط دهه ۱۹۸۵ ایجاد کرد که روی سطح باکتریوفاژ، پپتیدها و پروتئینهای کوچک فیوژشده با پروتئین pIII فاژ رشتهای را نمایش داد. تکنیکی که برای نمایش پپتیدها یا پروتئینهای خارجی روی سطح ذره فاژ به کار میرود، نمایش فاژ نامیده میشود [8].
از آن زمان تاکنون، سیستمهای مختلف نمایش فاژ برای بیان پروتئینهای خارجی در سطح فاژ توسعه یافته است. با این حال، اندازه پروتئین خارجی برای نمایش در سطح فاژ نسبتاً محدود است. سیستم نمایش سطح سلولی میکروبی برای حل این مشکل و برای چندین کاربرد منحصربهفرد دیگر توسعه یافته است. در مورد نمایش سطح سلولی باکتری، سیستمهای نمایش باکتریایی که ساخت آنها بر اساس پروتئینهای OmpA و LamB باکتری E. coli است، برای اولین بار در سال 1986 گزارش شد. از آن زمان، بسیاری از سیستمهای نمایش سطحی باکتریهای مختلف با استفاده از هر ۲ باکتری گرم منفی و گرم مثبت به عنوان سویه میزبان توسعه یافت [9].
بودر و ویتراپ برای اولین بار نمایش سطحی مخمر را در سال ۱۹۹۷ معرفی کردند [10]. ارگانیسمی که اغلب برای نمایش سطحی مخمر استفاده میشود، ساکارومایسس سرویزیه است [۹]. مشکل اصلی درباره استفاده از این سیستمها به نیاز پروتئین کایمریک برای عبور از غشای سیتوپلاسمی مربوط میشود. هر پروتئین کایمر قادر به عبور از این مانع نیست که موجب شکست نمایش سطحی میشود. بیشتر این محدودیتها را میتوان با استفاده از اندوسپورهای باکتریایی برطرف کرد [2].
نمونههای کلاسیک میکروارگانیسمهای تشکیلدهنده اسپور، باکتریهایی از جنس باسیلوس هستند. تشکیل اندوسپورها یک استراتژی است که توسط این باکتریها برای زنده ماندن در شرایط نامطلوب و محدودکننده رشد استفاده میشود. باسیلوس یک باکتری هوازی شناخته شده است که به طور گسترده برای تولید پروتئینهای صنعتی استفاده میشود. این باکتری به عنوان یک میکروارگانیسم GRAS (به طور کلی به عنوان میکروارگانیسم ایمن شناخته میشود) طبقهبندی میشود، نیازهای تغذیهای کمی دارد و به عنوان یک میکروارگانیسم گرم مثبتِ مدل عمل میکند [2].
فناوری نمایش سطحی اسپور روشی برای لنگر انداختن پروتئینهای عملکردی روی سطح اسپور، از امیدوارکنندهترین رویکردها برای بیان پروتئینهای هترولوگ با فعالیت و پایداری بالا در نظر گرفته میشود و مزایای متعددی دارد. اول، اسپورها در برابر شرایط سخت محیطی (مانند گرما، پرتو و مواد شیمیایی) مقاوم هستند و این امر به استفاده و پایداری پروتئینهای اگزوژن در محیطهای سخت کمک میکند. دوم، اسپورها در سیتوپلاسم سلولهای باکتری ساخته میشود؛ بنابراین پروتئین هترولوگ برای اتصال به اسپور نیاز به عبور از غشای سیتوپلاسمی ندارد. سوم، چاپرونهای مولکولی فعال موجود در سیتوپلاسم باکتریهای تولیدکننده اسپور میتواند به طور مناسب ترشح و بیان مناسب پروتئینهای هترولوگ خارجی را تسهیل کند. در حال حاضر، از این فناوری برای اهداف مختلفی مانند تولید آنزیمها، واکسنهای خوراکی، داروها و پروتئینهای مولتی مریک و همچنین کنترل آلودگیهای محیطی استفاده میشود [11، 12].
در میان گونههای مختلف باسیلوس سوبتیلیس که یک میکروارگانیسم صنعتی بسیار مهم است، به دلیل دانش دقیق از ساختار اسپور و در دسترس بودن و سهولت ابزارهای ژنتیکی پیشرفته و دادههای ژنومیک که ساخت اسپورهای نوترکیب را تسهیل میکند، توجه زیادی را به خود جلب کرده است [1]. باسیلوس سوبتیلیس یک باکتری معمولی گرم مثبت و میلهای شکل با محتوای کم G+C در ژنوم است که اغلب به عنوان ارگانیسم مدل برای مطالعه تمایز سلولی و مورفوژنز در میکروبیولوژی استفاده میشود.
برخی از متداولترین محیطهای اکولوژیکی آن شامل خاک، ریشه گیاهان و دستگاه گوارش حیوانات است. قبلاً اعتقاد بر این بود که باسیلوس سوبتیلیس هوازی اجباری است، اما شواهد تجربی ثابت کردند که این باکتری با استفاده از نیترات به جای اکسیژن به عنوان گیرنده الکترون، قادر به رشد بیهوازی نیز است. اسپورهای باسیلوس سوبتیلیس اشکال خفته این میکروارگانیسم هستند که به دلیل مقاومت در برابر شرایط سخت محیطی شناخته شدهاند. اسپورهای باسیلوس سوبتیلیس نسبتاً بهراحتی خالص میشوند و به شکل بیضیشکل و به اندازه 0/8 تا 1/2 میکرومتر طول دارند [13، 14].
همچنین تولید اسپور که مقاومترین شکل حیاتی روی زمین است، تضمینکننده حفظ این سویه حتی در شرایط سخت محیطی است. توانایی رشد در محیط کشت ساده و ارزان قیمت و نیز رشد سریع باعث شده که از فرم رویشی این سویه و اسپور آن برای نمایش سطحی پروتئینهای هترولوگ و کاربرد در صنایع مختلف، ازجمله تهیه واکسن استفاده زیادی شود [15-19].
ایستیکاتو و همکاران در سال 2001 استفاده از اسپور باسیلوس سوبتیلیس را برای نمایش سطحی پروتئین از زمان اولین کاربرد موفقیتآمیز به طور گسترده گزارش کردهاند [1]. اصل اساسی تکنیک نمایش در سطح اسپور افزایش عملکرد و پایداری پروتئینهای هدف با لنگر انداختن چنین پروتئینهای عملکردی اگزوژن بر روی سطح اسپورها با استفاده از تکنیکهای مختلف است. در این فناوری، یک ناقل بیانی نوترکیب معمولاً با معرفی یک ژن هدف و ژن کدکننده پروتئین پوششی اسپور (به نام پروتئین لنگر) تحت کنترل پروموتر خود ساخته میشود که سپس به سویه میزبان منتقل میشود. پروتئین یا پلی پپتید اگزوژن روی سطح اسپور میزبان با القای تشکیل اسپور در یک محیط کشت خشن بیان میشود. این اسپورها مقاومت بالایی در برابر محیطهای سخت دارند و پروتئینهای اگزوژن متصل به سطح اسپور نیز چنین مقاومت تنشی را به دست میآورند [11].
برای نمایش در سطح اسپور باسیلوس سوبتیلیس از ۲ رویکرد اصلی استفاده میشود: 1. رویکرد نوترکیب و 2. رویکرد غیرنوترکیب. رویکرد نوترکیب نیاز به اصلاح ژنوم باکتری برای بیان پروتئین مورد نظر به عنوان فیوژن با پروتئین پوشش اسپور دارد و رویکرد غیرنوترکیب مبتنی بر جذب مستقیم پروتئینهای هترولوگ در سطح اسپور یا لنگر انداختن پروتئینهای اگزوژن روی سطح اسپور با یک عامل اتصال متقابل است [12].
هدف از انجام این مطالعه، مروری جامع بر کاربرد اسپور باسیلوس سوبتیلیس در تولید واکسنهای مخاطی است.
مواد و روشها
مطالعه حاضر یک مطالعه مروری نظاممند است. جستوجوی مقالات با کلیدواژههای Bacillus Subtilis Spore ،Mucosal Vaccine و Surface Display و واژههای کلیدی معادل آن به زبان فارسی، «اسپور باسیلوس سوبتیلیس»، «واکسن مخاطی»، و «نمایش سطحی» در پایگاههای دادهای گوگل اسکولار، اسکوپوس و پابمد انجام شد. در این مرحله، حدود 5000 مقاله یافت شد. مطالعات یافتشده به تفکیک هر پایگاه داده بحث و بررسی شد. در مرحله اول، عنوان و چکیده مقالات بررسی شد، مقالات مشترک در پایگاه دادهها یا غیرمرتبط با موضوع کنار گذاشته و 360 مقاله انتخاب شد. سپس در ادامه، متن کامل مقالاتی که مرتبط با موضوع مطالعه ما بودند، مورد مطالعه بیشتر قرار گرفت. درنهایت، از 57 مقاله مرتبط با موضوع به عنوان رفرنس استفاده شد.
نتایج
اسپورزایی در باسیلوس سوبتیلیس
اسپور سویههای مختلف باسیلوس در شرایط نامساعد محیطی و طی فرایند اسپورولاسیون تشکیل میشوند. این اسپورها برای حیات طولانیمدت سازگار شدهاند، چراکه به بسیاری از استرسهای محیطی مقاوم بوده و از لحاظ متابولیکی خاموش هستند. در باکتری باسیلوس سوبتیلیس فرایند اسپورزایی حدود 8 ساعت طول میکشد [20]. هنگامی که مواد غذایی کاهش پیدا میکند، اسپورزایی آغاز میشود. این فرایند با فعال شدن کینازهای حساس به هیستیدین (مانند KinA ،KinB و KinC) آغاز میشود. این کینازها منجر به فسفریلاسیون تنظیمکننده اصلی فرایند اسپورزایی، یعنی فاکتور رونویسی SpoOA میشوند. [21].
تقسیم نامتقارن سلول اسپورزا، اسپورانژیوم را تشکیل میدهد که از ۲ قسمت تشکیل شده است: سلول بزرگتر سلول مادری نام دارد و سلول کوچکتر که پیشاسپور نامیده میشود و درنهایت، تبدیل به اسپور میشود. مرحله بعد بلعیده شدن پیشاسپور توسط سلول مادری در فرایندی شبیه به فاگوسیتوز است. پس از تکمیل فرایند بلعیده شدن، پیشاسپور به صورت ۱ سلول ۲ غشایی درون سلول مادری پدیدار میشود. پس از آن ساختارهای حفاظتی اختصاصی مانند پوسته، کورتکس و پوشش اسپور به تدریج ساخته میشود [12].
دی پیکولینیک اسید که در سلول مادری سنتز میشود، به تدریج پیش اسپور را پر کرده و به از دست دادن آب آن کمک میکند، سلول مادری لیز شده و اسپور بالغ شکل میگیرد (تصویر شماره 1) [22]. در حضور محرک مناسب، مثلاً وجود مواد غذایی در محیط، به ویژه L-آلانین، اسپورهای خاموش میتوانند طی فرایند جوانهزنی مجدداً حیات خود را بازیابند [23].
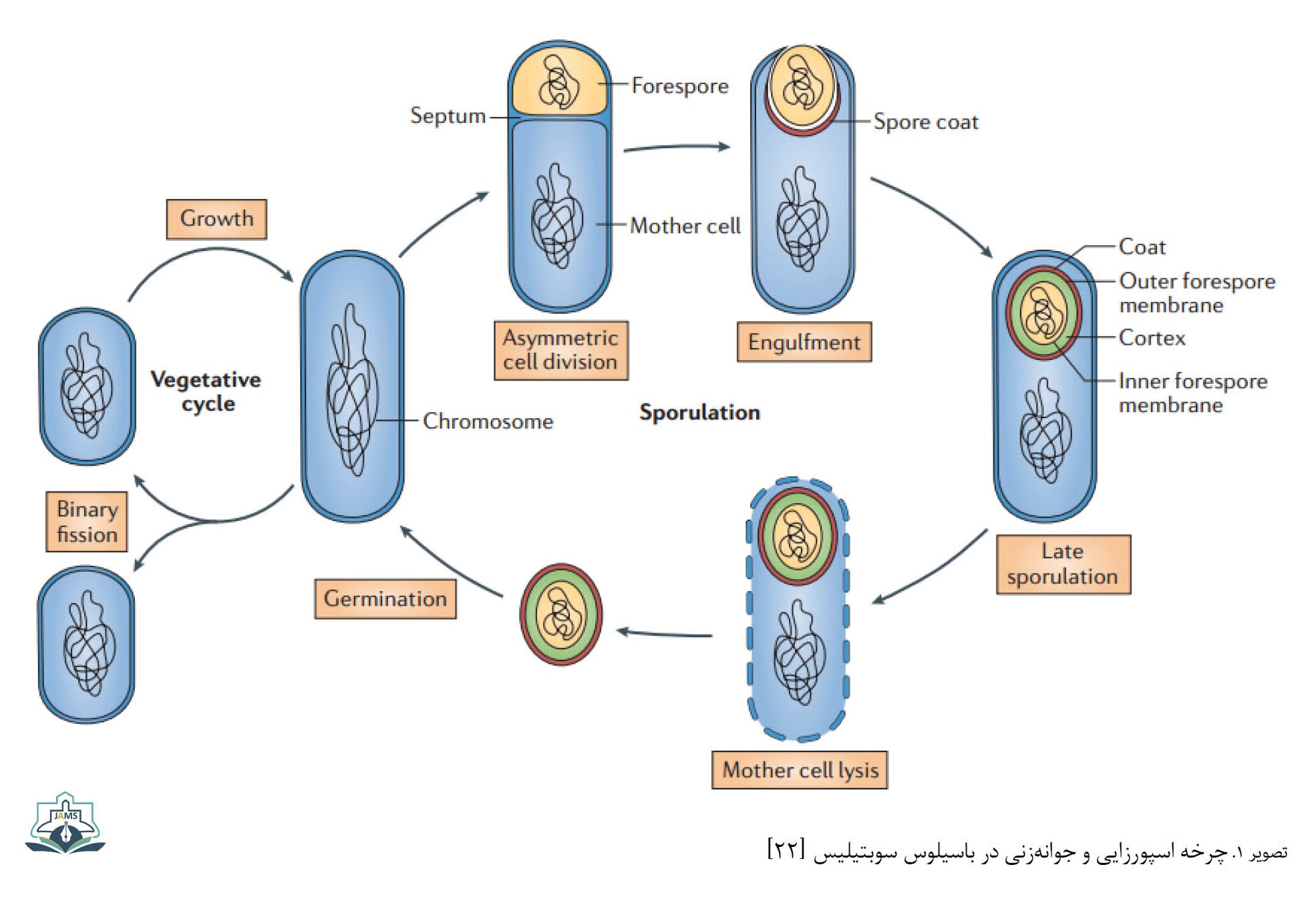
ساختار اسپور
ژنوم در ناحیه مرکزی اسپور که تا حدی دهیدراته شده است، قرار دارد و توسط پروتئینهای کوچک محلول در اسید به صورت فشرده درآمده است. قسمت عمده آب در ناحیه مرکزی با Ca+2-دی پیکولینیک اسید جایگزین شده است. در اطراف این ناحیه مرکزی از داخل به خارج غشای داخلی اسپور، دیواره سلول زایشی (لایه ضخیمی از پپتیدوگلیکان شبه دیواره سلول رویشی که در تصویر شماره 2 نشان داده نشده است)، کورتکس، غشای خارجی اسپور و پوشش اسپور قرار دارد. اغلب این ساختارها هنگام جوانه زدن اسپور به سرعت از بین میروند: پوشش ناپدید شده و کورتکس توسط هیدرولازهای دیواره سلولی تخریب میشود. دیواره سلول زایشی باقی میماند تا مبنای تشکیل دیواره سلول رویشی شود، غشای داخلی اسپور تبدیل به غشای پلاسمایی خواهد شد، در حالی که سرنوشت غشای خارجی اسپور کمتر شناخته شده است. ۳ لایه پوشش اسپور باسیلوس سوبتیلیس در میکروسکوپ الکترونی مشاهده شده است: پوشش داخلی لایه لایه، یک لایه پوشش خارجی ضخیمتر و لایهای که اخیراً شناسایی شده و پوسته نامیده میشود. [22].

پوشش اسپور از حداقل 80 پروتئین تشکیل شده است که توسط سلول مادری ساخته میشوند و طی بلعیده شدن در سطح اسپور قرار میگیرند [24]. در تصویر شماره 2 ساختار شماتیک اسپور و لایههای مختلف آن نشان داده شده است.
راهکارهای نمایش سطحی روی سطح اسپور
ایستیکاتو و همکاران، اولین مورد از نمایش ژنتیکی را روی اسپور باسیلوس سوبتیلیس در سال 2001 پیشنهاد کردند. در این مطالعه، CotB که از پروتئینهای پوشش اسپور است به قطعه 459 اسید آمینه از انتهای C ترمینال سم کزاز (TTFC) استفاده شد [1]. از آن زمان تاکنون، بسیاری از پروتئینهای هترولوگ و آنزیمها به صورت موفقیتآمیزی روی سطح اسپور باسیلوس سوبتیلیس نمایش داده شدهاند که اغلب آنها از روشهای ژنتیکی استفاده کردهاند تا پروتئین هدف را به یکی از پروتئینهای پوشش یا پوسته اسپور مانند CotB [25] ،[26] CotC ،[27] CotG ،[28] OxdD CotH [29] و [CotZ [30 متصل کنند.
هرچند روش ژنتیکی دارای برخی مزیتها مانند عدم نیاز به بیان و تخلیص پروتئین هدف است، اما میزان بیان پایین یا گاهی عدم بیان پروتئین این روش را برای کاربردهای صنعتی نامناسب میسازد. اشکال عمده دیگر در روش ژنتیکی آزاد شدن ارگانیسمهای نوترکیب زنده در طبیعت است که باعث ایجاد نگرانی در استفاده از این موجودات دستورزیشده ژنتیکی میشود [31]. برای غلبه بر این مشکلات، اخیراً استفاده از رویکرد غیرژنتیکی برای استفاده از اسپور به عنوان یک سیستم نمایش پیشنهاد شده است. در مطالعات مختلف NADPH سیتوکروم P450 ردوکتاز (CPR) پستانداران [32]، B-گالاکتوزیداز [31]، آلفاآمیلاز [33] و پروتئین A استافیلوکوکوس اورئوس [34] با استفاده از روشهای مختلف غیرژنتیکی مانند جذب سطحی و اتصالات کووالان روی سطح اسپور نمایش داده شدند.
کاربرد اسپور در توسعه واکسن
توسعه استراتژیهای واکسیناسیون همیشه به دلایل متعددی از اهمیت بالایی برخوردار بوده است: ایجاد سطوح بهتر ایمنی موضعی در برابر عوامل بیماریزا که عمدتاً از طریق سطوح مخاطی وارد بدن میشوند، ارائه مسیرهای تزریق بدون سوزن، ایجاد ایمنی بیشتر، کاهش عوارض جانبی و درنهایت، ارائه واکسنهای اقتصادی برای کشورهای در حال توسعه که در آن امکانات ذخیرهسازی و حملونقل غیربهینه میتواند از برنامههای ایمنسازی مؤثر جلوگیری کند. ایمنسازی خوراکی با آنتیژنهای محلول باعث ایجاد پاسخهای ایمنی ضعیف به دلیل تخریب آنتیژن در معده، جذب محدود و ایجاد تحمل میشود.
سیستمهای باکتریایی برای ارائه آنتیژن هترولوگ توجه قابلتوجهی را به خود جلب کردهاند، اما از آنجا که این سیستمها عمدتاً به پاتوژنهای ضعیفشده زنده مانند سالمونلا و مایکوباکتریوم متکی هستند، نگرانیهای ایمنی قابلتوجهی باقی میماند. باکتری گرم مثبت باسیلوس سوبتیلیس به طور گسترده به عنوان یک سیستم پروکاریوتی مطالعه شده است. این ارگانیسم به عنوان یک پاتوژن در نظر گرفته نمیشود و به عنوان یک غذای جدید طبقهبندی میشود که در حال حاضر به عنوان یک پروبیوتیک برای مصرف انسان و حیوان به کار میرود. اسپور بالغ باسیلوس، هنگامی که از سلول مادرش آزاد میشود، میتواند صدها و بلکه هزاران سال به شکل غیرفعال متابولیکی زنده بماند. [35].
از سوی دیگر، توسعه واکسنهای مخاطی به شدت به یک سیستم تحویل کارآمد متکی است و در طول سالها، رویکردهای مختلفی بر اساس فاژها، باکتریها یا نانوذرات مصنوعی برای نمایش و تحویل آنتیژنها پیشنهاد شده است [36]. در سالهای اخیر نحوه تحویل واکسن به بدن یک زمینه مهم تحقیقاتی در توسعه واکسن بوده است [37].
واکسنهای مخاطی مزیتهای بالقوه نسبت به واکسنهای تزریقی دارند، ازجمله عدم خطر انتقال بیماریها از طریق خون، عدم نیاز به پرسنل آموزشدیده برای مدیریت و امکان برانگیختن پاسخ ایمنی در محل ورود بیشتر پاتوژنها. با این حال، با وجود این مزایای بالقوه و موفقیت اولیه با واکسن خوراکی فلج اطفال بیش از 50 سال پیش، واکسنهای تزریقی به طور گستردهای رایجتر از واکسنهای مخاطی هستند و این تا حدی به دلیل برخی از معایب مرتبط با واکسنهای مخاطی موجود است، مانند جذب ضعیف آنتیژن، تخریب سریع آنتیژن در سطوح مخاطی و فقدان ادجوانتهای مخاطی ایمن و مؤثر.
سازمانهای بهداشت عمومی، جامعه علمی را به توسعه سیستمهای کارآمد برای رساندن آنتیژنها به محلهای مخاطی که جذب توسط سلولهای ارائهدهنده آنتیژن محلی را تسهیل میکنند، ترغیب کردهاند. اسپور باسیلوس سوبتیلیس گزینه مناسبی برای طراحی واکسنهای مخاطی است. اسپور خواص مقاومت منحصربهفردی را ارائه میدهد و میتواند در دمای شدید، خشک شدن و قرار گرفتن در معرض حلالها و سایر مواد شیمیایی مضر زنده بماند. این ویژگیهای منحصربهفرد اسپور را به وسیلهای جذاب برای انتقال آنتیژنهای هترولوگ یا درواقع، هر مولکول زیستفعال به محیطهایی مانند دستگاه گوارش تبدیل میکند [36].
در سال 2001، اولین گامها در توسعه اندوسپورهای باسیلوس سوبتیلیس برای تولید واکسن جدید گزارش شد. [1]. در سال 2003، کزاز به عنوان یک بیماری الگو برای یک مطالعه انتخاب شد. این مطالعه تأیید کرد که اسپورها را میتوان به عنوان واکسنهای خوراکی (و داخل بینی) مهندسی کرد و توسعه داد. سهولت دستکاری ژنتیکی، ذخیرهسازی طولانیمدت و سهولت تولید میتواند اسپور باسیلوس سوبتیلیس را به یک ناقل جذاب برای تولید واکسن نسل دوم تبدیل کند. نتایج آنها قویاً نشان میدهد که اسپورها به عنوان ناقل آنتیژنهای هترولوگ برای واکسیناسیون خوراکی و احتمالاً استنشاقی مناسب هستند [35].
در مطالعه دیگری در سال 2006، اسپورهای نوترکیب بیانکننده قطعاتی از آنتیژن محافظ باسیلوس آنتراسیس از طریق داخل صفاقی به موشها تزریق و موشهای ایمنشده در برابر بیماری سیاهزخم ایجاد کردند. این واکسن، اساس واکسنهای غیرسلولی فعلی برای استفاده انسانی را تشکیل داد [38].
در سال 2007 نشان داده شد اسپور باسیلوس سوبتیلیس هر ۲ پاسخ ایمنی اختصاصی هومورال و سلولی را هم به صورت سیستمیک و هم به صورت مخاطی افزایش میدهد. نتایج این مطالعه نشان میدهد اسپور باسیلوس سوبتیلیس میتواند به عنوان یک میکروذره طبیعی با فعالیت ادجوانتی، کاربرد بالینی زیادی داشته باشد [39].
در مطالعهای در سال 2008، از اسپورها برای واکسیناسیون خوراکی موشها در مقابله با دُز کشنده سم آلفا کلستریدیوم پرفرجنس استفاده شد. نتیجه این تحقیق تولید اسپورهایی بود که میتوانستند برای واکسیناسیون علیه سم آلفا کلستریدیوم پرفرجنس برای محافظت در برابر قانقاریای گازی در انسان و آنتریت نکروزه در طیور استفاده شوند [40].
سپس در مطالعه دیگری، دانشمندان تلاش کردند تا اسپورها را برای رساندن آنتیژن به سیتوپلاسم سلول میزبان مهندسی کنند. این رویکرد میتواند برای تعدادی از اهداف پیشگیرانه و درمانی مانند واکسنهای ضدپاتوژنهای داخل سلولی، واکسیناسیون سلولهای دندریتیک و برای هدف قرار دادن داروهای ضدسرطان مفید باشد. [41].
در سال 2010، مشخص شد فعالیت ادجوانتی اسپورها با اتصال آنتیژن به سطح اسپور ایجاد میشود. اسپورها به عنوان حامل آنتیژن عمل میکنند و شباهت زیادی به خواص ادجوانتهای ریزذرات دارند. این مطالعه یک کاربرد خاص و جدید از اسپورهای باکتریایی را گزارش میکند که در آن آنتیژن میتواند روی سطح اسپور تثبیت شده و از طریق یک مسیر مخاطی وارد بدن شود و طیف وسیعی از پاسخهای ایمنی ایجاد میکند. بدین ترتیب اسپورها بدون نیاز به اصلاح ژنتیکی توانایی عمل به عنوان ادجوانت مخاطی را دارند. این دانشمندان همچنین نشان دادند ترکیبی از فعل و انفعالات الکترواستاتیک و آبگریز مسئول اتصال یک پروتئین به سطح اسپور است [42].
بین سالهای 2010 تا 2020، بسیاری مطالعات دیگر نیز روی اسپور باکتری باسیلوس سوبتیلیس و کاربرد آن در تولید واکسنهای مخاطی برای واکسیناسیون علیه بیماریهای آنفلوآنزا [43]، HIV [44]، عفونت Clonorchis Sinensis [45، 46]، بیماری سل [47]، عفونت سالمونلا [48] و سندروم لکه سفید [49] انجام شد که برخی از از روشهای ژنتیکی و برخی دیگر از روشهای غیرژنتیکی برای اتصال آنتیژن به سطح اسپور استفاده کردهاند.
در مطالعه دیگری در 2020، آنتیژن محافظ که یکی از ۳ عامل بیماریزای اصلی مرتبط با سیاهزخم است روی سطح اسپورهای باسیلوس سوبتیلیس نمایش داده شد. موشها به صورت خوراکی، داخل بینی، زیر زبانی یا داخل صفاقی با واکسن اسپور پروبیوتیک آنتیژن محافظ ایمن شدند. مشاهدات بالینی، تجزیهوتحلیل سرولوژیکی نشان داد موشهای واکسینهشده با واکسن اسپور آنتیژن محافظ از طرق مختلف، سطح تیتر آنتیبادی فعال، پروفایلهای ایزوتیپ و آنتیبادی خنثیکننده سم در سرم و IgA در بزاق را افزایش دادند [14].
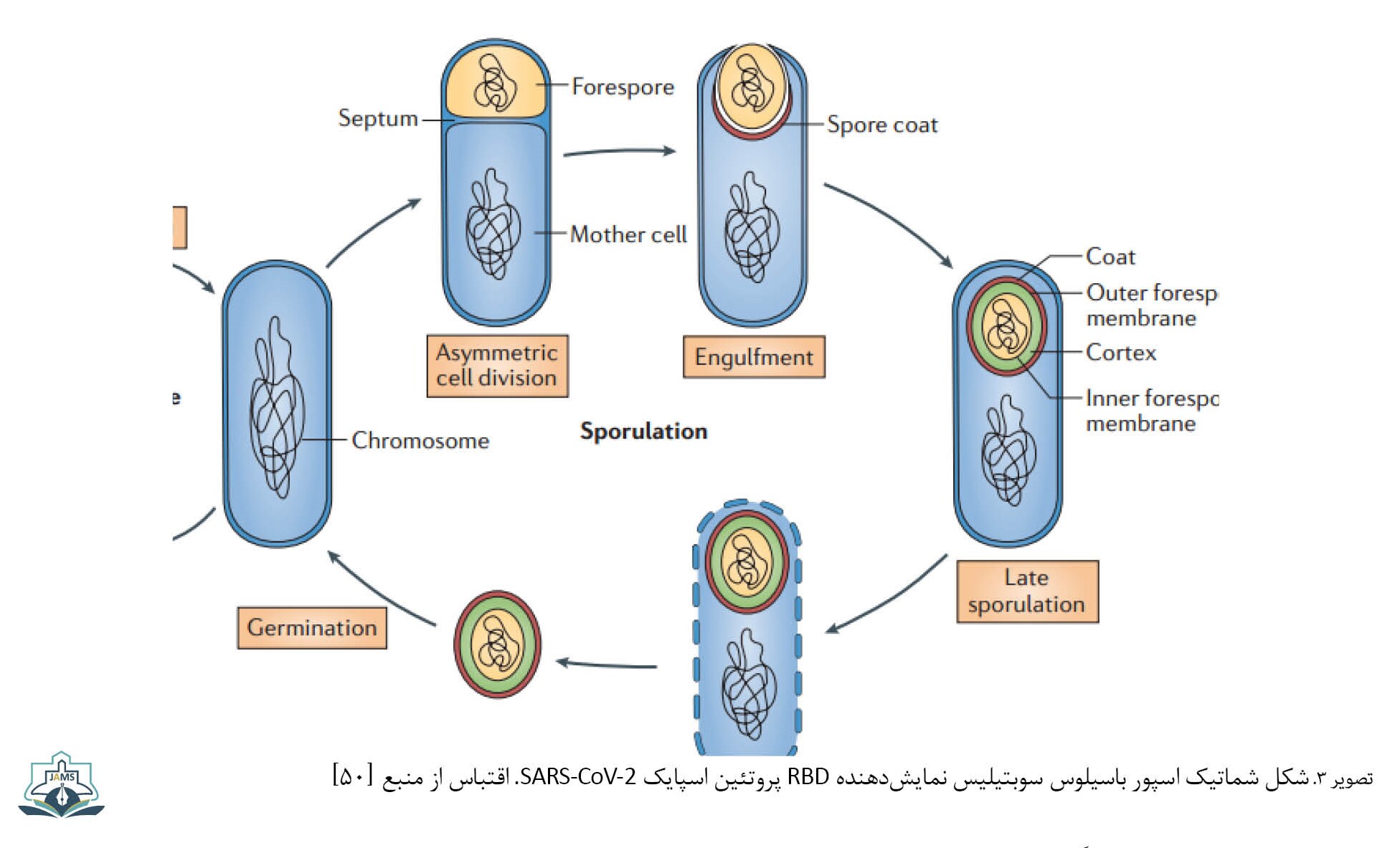
در همهگیری اخیر کووید-19 و به دلیل عدم وجود درمانهای دارویی مؤثر، توسعه و استفاده از واکسنهای مؤثر و بیخطر کووید-19 به یک استراتژی مهم برای کنترل شیوع این بیماری تبدیل شده است. در یکی از جدیدترین مطالعات، چانچائو سانگ و همکاران، دمین متصلشونده به گیرنده پروتئین اسپایک (SARS-CoV-19 (sRBD روی سطح اسپور باسیلوس سوبتیلیس نمایش دادند (تصویر شماره 3) و پس از تجویز خوراکی آن به عنوان واکسن، افزایش قابلتوجهی در آنتیبادی خنثیکننده علیه sRBD، هم در موش و هم در انسان مشاهده شد. دمین متصلشونده به گیرنده روی پروتئین اسپایک در پوشش ویروس بیان شده و هدف اصلی برای خنثیسازی توسط آنتیبادیها است. مزیت استفاده از ناقل باسیلوسی نسبت به آدنوویروس این است که باسیلوس سوبتیلیس نسبتاً ایمن است. علاوه بر این، انعقاد خون ایجاد نمیکند، زیرا ناقل باکتری وارد جریان خون نمیشود. واکسنهای سوبتیلیس هزینه تولید کمتری نیز دارند [50].
کاربرد اسپور به عنوان ادجوانت
با افزایش تعداد واکسنهای مبتنی بر پروتئین علیه پاتوژنهای عفونی، توسعه ادجوانتها برای واکسنها به یک حوزه مهم تحقیقاتی تبدیل شده است. مطالعات اخیر نشان داد اسپورهای باسیلوس سوبتیلیس زمانی که همزمان با پروتئینهای آنتیژنی خالصشده تجویز میشوند، ظرفیت ادجوانتی قوی دارند. مطالعات نشان دادهاند زمانی که اسپورهای باسیلوس سوبتیلیس همزمان با یک آنتیژن محلول تجویز شوند، نه تنها ایمنی ذاتی را
تقویت میکنند و در برابر عفونتهای تنفسی محافظت ایجاد میکنند، بلکه باعث افزایش آنتیبادی اختصاصی آنتیژن و تحریک پاسخهای ایمنی سلولی T میشوند. مزیت دیگر اسپورهای باسیلوس سوبتیلیس به عنوان ادجوانت در واکسنهای آنفلوآنزا شامل افزایش اثر واکسن و کاهش دفعات ایمنسازی مورد نیاز برای پاسخ ایمنی بهینه برای محافظت کامل است [51].
در مطالعه سونگ و همکاران، از اسپورهای گرمای کشتهشده باکتری باسیلوس سوبتیلیس به عنوان یک سیستم انتقال واکسن با خواص ادجوانتی مخاطی برای آنفلوآنزا استفاده و خواص آن ارزیابی شد [43].
همچنین در مطالعه دِ آلمیدا و همکاران، به منظور تولید یک واکسن علیه مالاریا از اسپور باسیلوس سوبتیلیس سویه KO7 فیوژ شده با پروتئین CSP نوترکیب پلاسمادیوم فالسی پاروم (rPfCSP) استفاده شد و پاسخ ایمنی هومورال ناشی از ایمیونیزاسیون از طریق مسیر بینی در موش Balb/C ارزیابی شد. نتایج این مطالعه نشان داد اسپورهای همراه با rPfCSP ایمنیزایی آنتیژن را افزایش میدهند و سطوح بالایی از IgG سرمی را القا میکنند. دادههای این مطالعه نشان داد استفاده از اسپور به عنوان ادجوانت میتواند پاسخ آنتیبادی بیشتر، سریعتر و طولانیتر را علیه آنتیژن PfCSP تحریک کند. علاوه بر این، نشان داده شد این رویکرد واکسن بسیار امیدوارکننده است، زیرا ممکن است پاسخ ایمنی متعادل Th1/Th2 را القا کند [52].
میزان ایمنیزایی واکسنهای مخاطی بر پایه اسپور
واکسیناسیون مخاطی از طریق تجویز خوراکی یا داخل بینی میتواند پاسخهای ایمنی مؤثری را در برابر عفونتهای مرتبط با موانع مخاطی مانند دستگاه گوارش (GIT=Gastrointestinal tract)، دستگاه تناسلی و حفره دهان ایجاد کند. اسپورهای باسیلوس سوبتیلیس برای ایمنسازی مخاطی به دلیل چندین ویژگی جذاب که شامل سابقه ایمنی استفاده از آنها در انسان و حیوان، مقاومت به pH اسیدی (برای تجویز خوراکی) و سهولت دستکاری ژنتیکی است، بررسی شده است. نکته مهم این است که اسپورهای باسیلوس سوبتیلیس میتوانند با سلولهای ایمنی تعامل داشته باشند و هنگام عبور از دستگاه گوارش باعث تولید پاسخ ایمنی محافظتی سیستم ایمنی بدن شوند [13].
مشخص شد اسپورهای باسیلوس سوبتیلیس ابزار ارزشمندی برای تحریک پاسخهای ایمنی قویتر با افزایش نمایش آنتیژن هستند [53]. علاوه بر پاسخهای ایمنی به واسطه آنتیبادی، مطالعات بیشتر نشان داد اسپورهای نوترکیب پاسخ سلولی سلولهایT CD4+/CD8+ اختصاصی آنتیژن را تقویت میکنند. مطالعات دیگر نشان دادهاند اسپور باسیلوس سوبتیلیس توسط TLR2 ،TLR4 و TLR9 نیز شناخته میشود و میتواند پاسخهای Th1/Th2 را با حضور IgG2a و IgG1 در سرم موشهای ایمنشده القا کند [43].
مقایسه ایمنیزایی واکسنهای مخاطی بر پایه اسپور با سایر واکسنها
واکسنهای دارای مجوز در حال حاضر از طریق یکی از ۵ مسیر اصلی تجویز میشوند که تجویز عضلانی، رایجترین آن است و چندین واکسن مانند هپاتیت A و B، هاری، آنفلوآنزا، دیفتری، کزاز و سیاه سرفه با این روش تزریق میشود. مسیرهای زیرجلدی و داخل پوستی نیز رایج است و به ترتیب برای واکسیناسیون سرخک، اوریون، سرخجه، تب زرد و (واکسن ضدبیماری سل)- هاری استفاده میشود. ۲ مسیر باقیمانده آنتیژنها را به سطوح مخاطی بینی یا روده میرساند. از راه داخل بینی، برای مثال، برای ویروسهای آنفلوآنزای ضعیفشده زنده استفاده میشود، در حالی که مسیر دهانی برای واکسیناسیون فلج اطفال، وبا، روتاویروس و تب حصبه استفاده میشود [54].
مزایای زیادی وجود دارد که واکسنهای مخاطی را جایگزین جذابی برای واکسنهایی میکند که از راههای سیستمیک تجویز میشوند. ازجمله اینکه پاسخهای ایمنی محافظتی را میتوان در درگاههای مخاطی مربوط به ورود پاتوژن با تحویل واکسنها به مخاط القا کرد. نمونههای متعددی به وضوح اعتبار این استراتژی را نشان میدهد، ازجمله واکسنهای ویروس آنفلوآنزای غیرفعال یا ضعیفشده داخل بینی، واکسن فلج اطفال خوراکی و واکسنهای تضعیفشده خوراکی سالمونلا تیفی و ویبریو کلرا و بسیاری دیگر که در حال حاضر در حال توسعه علیه عفونتهای مختلف رودهای و تنفسی هستند [55].
همچنین نتایج حاصل از چندین مطالعه اخیر اهمیت پاسخهای ایمنی مخاطی در برابر SARS-CoV-2 را برجسته میکند. این مطالعات نشان میدهد که تجویز داخل بینی به عنوان یک استراتژی جذابتر برای تحریک پاسخ های ایمنی محافظتی اولیه در مخاط دستگاه تنفسی فوقانی قبل از اینکه SARS-CoV-2 جای پایی در دستگاه تنفسی تحتانی پیدا کند، است [56].
علاوه بر این، در اپیدمیهای ناشی از عفونتهای منتقله از طریق مخاط، ایمنسازی انبوه از راههای مخاطی احتمالاً عملیتر و کمهزینهتر از ایمنسازی از راههای سیستمیک است. همچنین کاهش هزینه واکسنهای مخاطی در هر ۲ سطح تولید و تحویل محقق میشود. خلوص واکسنهای تحویل دادهشده از طریق مخاط، ازجمله آلودگی به اندوتوکسین، نسبت به واکسنهای تزریقی اهمیت کمتری دارد. برخی از واکسنهای مخاطی نیازی به نگهداری در دمای پایین ندارند و زمانی که در دمای محیط برای مدت طولانی نگهداری شوند، پایدار و کاملاً ایمونوژن باقی میمانند. درنهایت، تحویل واکسن مخاطی به سرنگها و سوزنهای استریل یا پرسنل آموزشدیده برای استفاده و دفع آنها نیاز ندارد، اگرچه ممکن است دستگاههای اسپری یا سایر اعمالکنندهها برای تزریق داخل بینی و سایر راههای تزریق مورد نیاز باشد [55].
بحث
مطالعه حاضر نشان داد واکسنهای مخاطی مبتنی بر اسپور مزایای بیشماری مانند کمک به واکسیناسیون انبوه با افزایش سهولت و سرعت تحویل، کاهش هزینهها با حذف مراحل تصفیه و تجویز منعطف از طریق مسیرهای مخاطی یا دهانی و سیستمهای تحویل واکسن بدون سوزن و بدون یخچال را ارائه میدهند [57].
یکی دیگر از ویژگیهای منحصربهفرد واکسنهای مخاطی مبتنی بر اسپور این است که اسپورها نانوساختارهایی در مقیاس زیر میکرون دارند که به آنها اجازه میدهد تا به عنوان ادجوانتهای ذرهای مؤثر عمل کنند. ادجوانتهای ذرهای به طور مؤثر سلولهای ارائهدهنده آنتیژن را هدف قرار میدهند و پس از درونی شدن در سلول، توسط مجموعه سازگاری بافتی اصلی کلاس I و کلاس II پردازش میشوند که منجر به ارائه آنتیژن در سطح APC میشود.
همچنین مطالعاتی که خاصیت ادجوانتی اسپورهای باسیلوس سوبتیلیس را بررسی میکنند، نشان میدهند که اثرات ادجوانتی قوی زمانی مشاهده میشوند که اسپورها با آنتیژنهای پروتئینی که مخلوط یا جذبشده روی سطح پوشش اسپور هستند، تجویز میشوند. به علاوه، مشخص شده که اندازه ذرات اسپور برای تقویت ایمنی مخاطی مناسب است؛ بنابراین انعطافپذیری اسپورها، همراه با یک مسیر مخاطی تحویل، واکسنهای اسپور را به کاندیدایی امیدوارکننده تبدیل میکند، به ویژه زمانی که تولید انبوه و واکسیناسیون در مقیاس بزرگ به فوریت مورد نیاز باشد [58].
محدودیتهای واکسنهای مخاطی بر پایه اسپور باسیلوس سوبتیلیس
با وجود تمام مزایای واکسنهای مخاطی مبتنی بر اسپور، استفاده از این نوع واکسنها معایبی نیز دارد؛ بنابراین در استفاده از آنها باید به نکات ایمنی و اخلاقی توجه کرد. چنانچه اسپورها به طور کامل غیرفعال نشده باشند و در شرایط بهینه رشد قرار گیرند، به فرم فعال باکتریایی تبدیل میشوند؛ بنابراین باید مشخص باشد که چه نسبتی از اسپورها ممکن است جوانه بزنند و آیا این امر قابل کنترل است یا نه؟ همچنین واکسنهای مخاطی باید بر مشکلات مرتبط با جذب ضعیف یا تخریب در سیستم گوارش غلبه کنند [54].
مشکل دیگر استفاده از اسپورها به عنوان ناقل واکسن در مورد واکسنهای حیوانی است. اسپورهای نوترکیبی که به عنوان واکسن در حیوانات استفاده میشوند، میتوانند از طریق مدفوع، وارد محیط زیست شوند و این امر موجب تجمع اسپورهای نوترکیب در محیط میشود. از سوی دیگر، اگرچه باکتری باسیلوس سوبتیلیس به عنوان یک باکتری ایمن شناخته میشود، اما ممکن است گاهی با عفونتهای فرصت طلب مرتبط باشد؛ بنابراین باید از گونههای باکتری کاملاً شناخته شده استفاده کرد.
نتیجهگیری
به طور کلی اسپورها مقاومت خوبی در برابر استرس دارند؛ بنابراین واکسنهایی که با این روش تولید میشوند، میتوانند محیط اسیدی دستگاه گوارش را تحمل کنند و ماندگاری طولانیمدت داشته باشند. آنها میتوانند به آرامی از مخاط دستگاه گوارش عبور کنند و به سرعت سیستم ایمنی بدن را وادار به تولید یک پاسخ ایمنی محافظتی کنند. علاوه بر این، استفاده از اسپور به عنوان حامل واکسن میتواند کارایی پاسخ ایمنی را بهبود ببخشد.
واکسنهای خوراکی باسیلوس سوبتیلیس سهم قابلتوجهی در پیشگیری و درمان کووید-۱۹ در آینده خواهند داشت. هر چند در حال حاضر، هیچ واکسن در دسترس تجاری از یک ناقل باسیلوسی وجود ندارد. اسپورهای باسیلوس سوبتیلیس به عنوان ناقل واکسنها میتوانند کمک قابل توجهی در پیشگیری و درمان بیماریها در آینده داشته باشند.
در پژوهش حاضر سعی شد از تمام منابع مرتبط با موضوع استفاده شود، اما زیاد بودن تعداد منابع و احتمال از دست دادن برخی از آنها و نیز عدم دسترسی به متن کامل برخی از مقالات، ازجمله محدودیتهای این مطالعه است. همچنین باکتری باسیلوس سوبتیلیس و اسپور آن کاربردهای بسیاری دارد که در این پژوهش تنها به قسمتی از آن اشاره شده است.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
همه اصول اخلاقی در نگارش این مقاله، طبق دستورالعمل کمیته ملی اخلاق و آییننامه COPE رعایت شده است.
حامی مالی
این پژوهش هیچگونه کمک مالی از سازمانهای دولتی، خصوصی و غیرانتفاعی دریافت نکرده است.
مشارکت نویسندگان
طرح ایده اولیه: غلامرضا احمدیان؛ مطالعه، پژوهش و نگارش مقاله: سمیرا قائدمحمدی، حورا بحرالعلوم؛ بازبینی: غلامرضا احمدیان، سمیرا قائدمحمدی.
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
نمایش سطحی یک تکنیک مولکولی است که توسط آن پپتیدها و پروتئینهای هترولوگ در سطح خارجی باکتریوفاژها، سلولها یا اسپورها تثبیت میشوند. این تکنیک در حال تبدیل شدن به یک ابزار تحقیقاتی در زمینههای مختلف میکروبیولوژی، زیستشناسی مولکولی، واکسنشناسی و بیوتکنولوژی است. این رویکرد مبتنی بر ایده استفاده از پروتئینهای سطحی طبیعی به عنوان لنگر برای هدفگیری پروتئینهای مورد نظر است که پروتئینهای مسافری نیز نامیده میشوند.
رایجترین رویکردها برای نمایش سطحی پروتئین شامل استفاده از سلولهای مخمر یا پروکاریوتی، فاژها و اسپورهای باکتریایی است. فناوری نمایش سطحی طیف وسیعی از کاربردهای بیوتکنولوژیکی و صنعتی را نشان داده است. از جمله این کاربردها شامل توسعه واکسنهای زنده، غربالگری کتابخانههای پپتیدی، تولید آنتیبادی، جاذبهای زیستی برای حذف مواد شیمیایی مضر و فلزات سنگین، بیوکاتالیستهای کل سلولی با بیحرکت کردن آنزیمها، توسعه حسگرهای زیستی و غیره هستند [1، 2].
اولین گزارشها درباره نمایش پروتئینهای هترولوگ روی سطح باکتریها در سال 1986 مطرح شد [3، 4]. پس از آن، سیستمهای نمایشی متنوع دیگری نیز روی سطح مخمر، باکتریهای گرم مثبت و باکتریهای گرم منفی گسترش یافت [5-7]. اولین سیستم بیان سطحی را جورج اسمیت در اواسط دهه ۱۹۸۵ ایجاد کرد که روی سطح باکتریوفاژ، پپتیدها و پروتئینهای کوچک فیوژشده با پروتئین pIII فاژ رشتهای را نمایش داد. تکنیکی که برای نمایش پپتیدها یا پروتئینهای خارجی روی سطح ذره فاژ به کار میرود، نمایش فاژ نامیده میشود [8].
از آن زمان تاکنون، سیستمهای مختلف نمایش فاژ برای بیان پروتئینهای خارجی در سطح فاژ توسعه یافته است. با این حال، اندازه پروتئین خارجی برای نمایش در سطح فاژ نسبتاً محدود است. سیستم نمایش سطح سلولی میکروبی برای حل این مشکل و برای چندین کاربرد منحصربهفرد دیگر توسعه یافته است. در مورد نمایش سطح سلولی باکتری، سیستمهای نمایش باکتریایی که ساخت آنها بر اساس پروتئینهای OmpA و LamB باکتری E. coli است، برای اولین بار در سال 1986 گزارش شد. از آن زمان، بسیاری از سیستمهای نمایش سطحی باکتریهای مختلف با استفاده از هر ۲ باکتری گرم منفی و گرم مثبت به عنوان سویه میزبان توسعه یافت [9].
بودر و ویتراپ برای اولین بار نمایش سطحی مخمر را در سال ۱۹۹۷ معرفی کردند [10]. ارگانیسمی که اغلب برای نمایش سطحی مخمر استفاده میشود، ساکارومایسس سرویزیه است [۹]. مشکل اصلی درباره استفاده از این سیستمها به نیاز پروتئین کایمریک برای عبور از غشای سیتوپلاسمی مربوط میشود. هر پروتئین کایمر قادر به عبور از این مانع نیست که موجب شکست نمایش سطحی میشود. بیشتر این محدودیتها را میتوان با استفاده از اندوسپورهای باکتریایی برطرف کرد [2].
نمونههای کلاسیک میکروارگانیسمهای تشکیلدهنده اسپور، باکتریهایی از جنس باسیلوس هستند. تشکیل اندوسپورها یک استراتژی است که توسط این باکتریها برای زنده ماندن در شرایط نامطلوب و محدودکننده رشد استفاده میشود. باسیلوس یک باکتری هوازی شناخته شده است که به طور گسترده برای تولید پروتئینهای صنعتی استفاده میشود. این باکتری به عنوان یک میکروارگانیسم GRAS (به طور کلی به عنوان میکروارگانیسم ایمن شناخته میشود) طبقهبندی میشود، نیازهای تغذیهای کمی دارد و به عنوان یک میکروارگانیسم گرم مثبتِ مدل عمل میکند [2].
فناوری نمایش سطحی اسپور روشی برای لنگر انداختن پروتئینهای عملکردی روی سطح اسپور، از امیدوارکنندهترین رویکردها برای بیان پروتئینهای هترولوگ با فعالیت و پایداری بالا در نظر گرفته میشود و مزایای متعددی دارد. اول، اسپورها در برابر شرایط سخت محیطی (مانند گرما، پرتو و مواد شیمیایی) مقاوم هستند و این امر به استفاده و پایداری پروتئینهای اگزوژن در محیطهای سخت کمک میکند. دوم، اسپورها در سیتوپلاسم سلولهای باکتری ساخته میشود؛ بنابراین پروتئین هترولوگ برای اتصال به اسپور نیاز به عبور از غشای سیتوپلاسمی ندارد. سوم، چاپرونهای مولکولی فعال موجود در سیتوپلاسم باکتریهای تولیدکننده اسپور میتواند به طور مناسب ترشح و بیان مناسب پروتئینهای هترولوگ خارجی را تسهیل کند. در حال حاضر، از این فناوری برای اهداف مختلفی مانند تولید آنزیمها، واکسنهای خوراکی، داروها و پروتئینهای مولتی مریک و همچنین کنترل آلودگیهای محیطی استفاده میشود [11، 12].
در میان گونههای مختلف باسیلوس سوبتیلیس که یک میکروارگانیسم صنعتی بسیار مهم است، به دلیل دانش دقیق از ساختار اسپور و در دسترس بودن و سهولت ابزارهای ژنتیکی پیشرفته و دادههای ژنومیک که ساخت اسپورهای نوترکیب را تسهیل میکند، توجه زیادی را به خود جلب کرده است [1]. باسیلوس سوبتیلیس یک باکتری معمولی گرم مثبت و میلهای شکل با محتوای کم G+C در ژنوم است که اغلب به عنوان ارگانیسم مدل برای مطالعه تمایز سلولی و مورفوژنز در میکروبیولوژی استفاده میشود.
برخی از متداولترین محیطهای اکولوژیکی آن شامل خاک، ریشه گیاهان و دستگاه گوارش حیوانات است. قبلاً اعتقاد بر این بود که باسیلوس سوبتیلیس هوازی اجباری است، اما شواهد تجربی ثابت کردند که این باکتری با استفاده از نیترات به جای اکسیژن به عنوان گیرنده الکترون، قادر به رشد بیهوازی نیز است. اسپورهای باسیلوس سوبتیلیس اشکال خفته این میکروارگانیسم هستند که به دلیل مقاومت در برابر شرایط سخت محیطی شناخته شدهاند. اسپورهای باسیلوس سوبتیلیس نسبتاً بهراحتی خالص میشوند و به شکل بیضیشکل و به اندازه 0/8 تا 1/2 میکرومتر طول دارند [13، 14].
همچنین تولید اسپور که مقاومترین شکل حیاتی روی زمین است، تضمینکننده حفظ این سویه حتی در شرایط سخت محیطی است. توانایی رشد در محیط کشت ساده و ارزان قیمت و نیز رشد سریع باعث شده که از فرم رویشی این سویه و اسپور آن برای نمایش سطحی پروتئینهای هترولوگ و کاربرد در صنایع مختلف، ازجمله تهیه واکسن استفاده زیادی شود [15-19].
ایستیکاتو و همکاران در سال 2001 استفاده از اسپور باسیلوس سوبتیلیس را برای نمایش سطحی پروتئین از زمان اولین کاربرد موفقیتآمیز به طور گسترده گزارش کردهاند [1]. اصل اساسی تکنیک نمایش در سطح اسپور افزایش عملکرد و پایداری پروتئینهای هدف با لنگر انداختن چنین پروتئینهای عملکردی اگزوژن بر روی سطح اسپورها با استفاده از تکنیکهای مختلف است. در این فناوری، یک ناقل بیانی نوترکیب معمولاً با معرفی یک ژن هدف و ژن کدکننده پروتئین پوششی اسپور (به نام پروتئین لنگر) تحت کنترل پروموتر خود ساخته میشود که سپس به سویه میزبان منتقل میشود. پروتئین یا پلی پپتید اگزوژن روی سطح اسپور میزبان با القای تشکیل اسپور در یک محیط کشت خشن بیان میشود. این اسپورها مقاومت بالایی در برابر محیطهای سخت دارند و پروتئینهای اگزوژن متصل به سطح اسپور نیز چنین مقاومت تنشی را به دست میآورند [11].
برای نمایش در سطح اسپور باسیلوس سوبتیلیس از ۲ رویکرد اصلی استفاده میشود: 1. رویکرد نوترکیب و 2. رویکرد غیرنوترکیب. رویکرد نوترکیب نیاز به اصلاح ژنوم باکتری برای بیان پروتئین مورد نظر به عنوان فیوژن با پروتئین پوشش اسپور دارد و رویکرد غیرنوترکیب مبتنی بر جذب مستقیم پروتئینهای هترولوگ در سطح اسپور یا لنگر انداختن پروتئینهای اگزوژن روی سطح اسپور با یک عامل اتصال متقابل است [12].
هدف از انجام این مطالعه، مروری جامع بر کاربرد اسپور باسیلوس سوبتیلیس در تولید واکسنهای مخاطی است.
مواد و روشها
مطالعه حاضر یک مطالعه مروری نظاممند است. جستوجوی مقالات با کلیدواژههای Bacillus Subtilis Spore ،Mucosal Vaccine و Surface Display و واژههای کلیدی معادل آن به زبان فارسی، «اسپور باسیلوس سوبتیلیس»، «واکسن مخاطی»، و «نمایش سطحی» در پایگاههای دادهای گوگل اسکولار، اسکوپوس و پابمد انجام شد. در این مرحله، حدود 5000 مقاله یافت شد. مطالعات یافتشده به تفکیک هر پایگاه داده بحث و بررسی شد. در مرحله اول، عنوان و چکیده مقالات بررسی شد، مقالات مشترک در پایگاه دادهها یا غیرمرتبط با موضوع کنار گذاشته و 360 مقاله انتخاب شد. سپس در ادامه، متن کامل مقالاتی که مرتبط با موضوع مطالعه ما بودند، مورد مطالعه بیشتر قرار گرفت. درنهایت، از 57 مقاله مرتبط با موضوع به عنوان رفرنس استفاده شد.
نتایج
اسپورزایی در باسیلوس سوبتیلیس
اسپور سویههای مختلف باسیلوس در شرایط نامساعد محیطی و طی فرایند اسپورولاسیون تشکیل میشوند. این اسپورها برای حیات طولانیمدت سازگار شدهاند، چراکه به بسیاری از استرسهای محیطی مقاوم بوده و از لحاظ متابولیکی خاموش هستند. در باکتری باسیلوس سوبتیلیس فرایند اسپورزایی حدود 8 ساعت طول میکشد [20]. هنگامی که مواد غذایی کاهش پیدا میکند، اسپورزایی آغاز میشود. این فرایند با فعال شدن کینازهای حساس به هیستیدین (مانند KinA ،KinB و KinC) آغاز میشود. این کینازها منجر به فسفریلاسیون تنظیمکننده اصلی فرایند اسپورزایی، یعنی فاکتور رونویسی SpoOA میشوند. [21].
تقسیم نامتقارن سلول اسپورزا، اسپورانژیوم را تشکیل میدهد که از ۲ قسمت تشکیل شده است: سلول بزرگتر سلول مادری نام دارد و سلول کوچکتر که پیشاسپور نامیده میشود و درنهایت، تبدیل به اسپور میشود. مرحله بعد بلعیده شدن پیشاسپور توسط سلول مادری در فرایندی شبیه به فاگوسیتوز است. پس از تکمیل فرایند بلعیده شدن، پیشاسپور به صورت ۱ سلول ۲ غشایی درون سلول مادری پدیدار میشود. پس از آن ساختارهای حفاظتی اختصاصی مانند پوسته، کورتکس و پوشش اسپور به تدریج ساخته میشود [12].
دی پیکولینیک اسید که در سلول مادری سنتز میشود، به تدریج پیش اسپور را پر کرده و به از دست دادن آب آن کمک میکند، سلول مادری لیز شده و اسپور بالغ شکل میگیرد (تصویر شماره 1) [22]. در حضور محرک مناسب، مثلاً وجود مواد غذایی در محیط، به ویژه L-آلانین، اسپورهای خاموش میتوانند طی فرایند جوانهزنی مجدداً حیات خود را بازیابند [23].

ساختار اسپور
ژنوم در ناحیه مرکزی اسپور که تا حدی دهیدراته شده است، قرار دارد و توسط پروتئینهای کوچک محلول در اسید به صورت فشرده درآمده است. قسمت عمده آب در ناحیه مرکزی با Ca+2-دی پیکولینیک اسید جایگزین شده است. در اطراف این ناحیه مرکزی از داخل به خارج غشای داخلی اسپور، دیواره سلول زایشی (لایه ضخیمی از پپتیدوگلیکان شبه دیواره سلول رویشی که در تصویر شماره 2 نشان داده نشده است)، کورتکس، غشای خارجی اسپور و پوشش اسپور قرار دارد. اغلب این ساختارها هنگام جوانه زدن اسپور به سرعت از بین میروند: پوشش ناپدید شده و کورتکس توسط هیدرولازهای دیواره سلولی تخریب میشود. دیواره سلول زایشی باقی میماند تا مبنای تشکیل دیواره سلول رویشی شود، غشای داخلی اسپور تبدیل به غشای پلاسمایی خواهد شد، در حالی که سرنوشت غشای خارجی اسپور کمتر شناخته شده است. ۳ لایه پوشش اسپور باسیلوس سوبتیلیس در میکروسکوپ الکترونی مشاهده شده است: پوشش داخلی لایه لایه، یک لایه پوشش خارجی ضخیمتر و لایهای که اخیراً شناسایی شده و پوسته نامیده میشود. [22].

پوشش اسپور از حداقل 80 پروتئین تشکیل شده است که توسط سلول مادری ساخته میشوند و طی بلعیده شدن در سطح اسپور قرار میگیرند [24]. در تصویر شماره 2 ساختار شماتیک اسپور و لایههای مختلف آن نشان داده شده است.
راهکارهای نمایش سطحی روی سطح اسپور
ایستیکاتو و همکاران، اولین مورد از نمایش ژنتیکی را روی اسپور باسیلوس سوبتیلیس در سال 2001 پیشنهاد کردند. در این مطالعه، CotB که از پروتئینهای پوشش اسپور است به قطعه 459 اسید آمینه از انتهای C ترمینال سم کزاز (TTFC) استفاده شد [1]. از آن زمان تاکنون، بسیاری از پروتئینهای هترولوگ و آنزیمها به صورت موفقیتآمیزی روی سطح اسپور باسیلوس سوبتیلیس نمایش داده شدهاند که اغلب آنها از روشهای ژنتیکی استفاده کردهاند تا پروتئین هدف را به یکی از پروتئینهای پوشش یا پوسته اسپور مانند CotB [25] ،[26] CotC ،[27] CotG ،[28] OxdD CotH [29] و [CotZ [30 متصل کنند.
هرچند روش ژنتیکی دارای برخی مزیتها مانند عدم نیاز به بیان و تخلیص پروتئین هدف است، اما میزان بیان پایین یا گاهی عدم بیان پروتئین این روش را برای کاربردهای صنعتی نامناسب میسازد. اشکال عمده دیگر در روش ژنتیکی آزاد شدن ارگانیسمهای نوترکیب زنده در طبیعت است که باعث ایجاد نگرانی در استفاده از این موجودات دستورزیشده ژنتیکی میشود [31]. برای غلبه بر این مشکلات، اخیراً استفاده از رویکرد غیرژنتیکی برای استفاده از اسپور به عنوان یک سیستم نمایش پیشنهاد شده است. در مطالعات مختلف NADPH سیتوکروم P450 ردوکتاز (CPR) پستانداران [32]، B-گالاکتوزیداز [31]، آلفاآمیلاز [33] و پروتئین A استافیلوکوکوس اورئوس [34] با استفاده از روشهای مختلف غیرژنتیکی مانند جذب سطحی و اتصالات کووالان روی سطح اسپور نمایش داده شدند.
کاربرد اسپور در توسعه واکسن
توسعه استراتژیهای واکسیناسیون همیشه به دلایل متعددی از اهمیت بالایی برخوردار بوده است: ایجاد سطوح بهتر ایمنی موضعی در برابر عوامل بیماریزا که عمدتاً از طریق سطوح مخاطی وارد بدن میشوند، ارائه مسیرهای تزریق بدون سوزن، ایجاد ایمنی بیشتر، کاهش عوارض جانبی و درنهایت، ارائه واکسنهای اقتصادی برای کشورهای در حال توسعه که در آن امکانات ذخیرهسازی و حملونقل غیربهینه میتواند از برنامههای ایمنسازی مؤثر جلوگیری کند. ایمنسازی خوراکی با آنتیژنهای محلول باعث ایجاد پاسخهای ایمنی ضعیف به دلیل تخریب آنتیژن در معده، جذب محدود و ایجاد تحمل میشود.
سیستمهای باکتریایی برای ارائه آنتیژن هترولوگ توجه قابلتوجهی را به خود جلب کردهاند، اما از آنجا که این سیستمها عمدتاً به پاتوژنهای ضعیفشده زنده مانند سالمونلا و مایکوباکتریوم متکی هستند، نگرانیهای ایمنی قابلتوجهی باقی میماند. باکتری گرم مثبت باسیلوس سوبتیلیس به طور گسترده به عنوان یک سیستم پروکاریوتی مطالعه شده است. این ارگانیسم به عنوان یک پاتوژن در نظر گرفته نمیشود و به عنوان یک غذای جدید طبقهبندی میشود که در حال حاضر به عنوان یک پروبیوتیک برای مصرف انسان و حیوان به کار میرود. اسپور بالغ باسیلوس، هنگامی که از سلول مادرش آزاد میشود، میتواند صدها و بلکه هزاران سال به شکل غیرفعال متابولیکی زنده بماند. [35].
از سوی دیگر، توسعه واکسنهای مخاطی به شدت به یک سیستم تحویل کارآمد متکی است و در طول سالها، رویکردهای مختلفی بر اساس فاژها، باکتریها یا نانوذرات مصنوعی برای نمایش و تحویل آنتیژنها پیشنهاد شده است [36]. در سالهای اخیر نحوه تحویل واکسن به بدن یک زمینه مهم تحقیقاتی در توسعه واکسن بوده است [37].
واکسنهای مخاطی مزیتهای بالقوه نسبت به واکسنهای تزریقی دارند، ازجمله عدم خطر انتقال بیماریها از طریق خون، عدم نیاز به پرسنل آموزشدیده برای مدیریت و امکان برانگیختن پاسخ ایمنی در محل ورود بیشتر پاتوژنها. با این حال، با وجود این مزایای بالقوه و موفقیت اولیه با واکسن خوراکی فلج اطفال بیش از 50 سال پیش، واکسنهای تزریقی به طور گستردهای رایجتر از واکسنهای مخاطی هستند و این تا حدی به دلیل برخی از معایب مرتبط با واکسنهای مخاطی موجود است، مانند جذب ضعیف آنتیژن، تخریب سریع آنتیژن در سطوح مخاطی و فقدان ادجوانتهای مخاطی ایمن و مؤثر.
سازمانهای بهداشت عمومی، جامعه علمی را به توسعه سیستمهای کارآمد برای رساندن آنتیژنها به محلهای مخاطی که جذب توسط سلولهای ارائهدهنده آنتیژن محلی را تسهیل میکنند، ترغیب کردهاند. اسپور باسیلوس سوبتیلیس گزینه مناسبی برای طراحی واکسنهای مخاطی است. اسپور خواص مقاومت منحصربهفردی را ارائه میدهد و میتواند در دمای شدید، خشک شدن و قرار گرفتن در معرض حلالها و سایر مواد شیمیایی مضر زنده بماند. این ویژگیهای منحصربهفرد اسپور را به وسیلهای جذاب برای انتقال آنتیژنهای هترولوگ یا درواقع، هر مولکول زیستفعال به محیطهایی مانند دستگاه گوارش تبدیل میکند [36].
در سال 2001، اولین گامها در توسعه اندوسپورهای باسیلوس سوبتیلیس برای تولید واکسن جدید گزارش شد. [1]. در سال 2003، کزاز به عنوان یک بیماری الگو برای یک مطالعه انتخاب شد. این مطالعه تأیید کرد که اسپورها را میتوان به عنوان واکسنهای خوراکی (و داخل بینی) مهندسی کرد و توسعه داد. سهولت دستکاری ژنتیکی، ذخیرهسازی طولانیمدت و سهولت تولید میتواند اسپور باسیلوس سوبتیلیس را به یک ناقل جذاب برای تولید واکسن نسل دوم تبدیل کند. نتایج آنها قویاً نشان میدهد که اسپورها به عنوان ناقل آنتیژنهای هترولوگ برای واکسیناسیون خوراکی و احتمالاً استنشاقی مناسب هستند [35].
در مطالعه دیگری در سال 2006، اسپورهای نوترکیب بیانکننده قطعاتی از آنتیژن محافظ باسیلوس آنتراسیس از طریق داخل صفاقی به موشها تزریق و موشهای ایمنشده در برابر بیماری سیاهزخم ایجاد کردند. این واکسن، اساس واکسنهای غیرسلولی فعلی برای استفاده انسانی را تشکیل داد [38].
در سال 2007 نشان داده شد اسپور باسیلوس سوبتیلیس هر ۲ پاسخ ایمنی اختصاصی هومورال و سلولی را هم به صورت سیستمیک و هم به صورت مخاطی افزایش میدهد. نتایج این مطالعه نشان میدهد اسپور باسیلوس سوبتیلیس میتواند به عنوان یک میکروذره طبیعی با فعالیت ادجوانتی، کاربرد بالینی زیادی داشته باشد [39].
در مطالعهای در سال 2008، از اسپورها برای واکسیناسیون خوراکی موشها در مقابله با دُز کشنده سم آلفا کلستریدیوم پرفرجنس استفاده شد. نتیجه این تحقیق تولید اسپورهایی بود که میتوانستند برای واکسیناسیون علیه سم آلفا کلستریدیوم پرفرجنس برای محافظت در برابر قانقاریای گازی در انسان و آنتریت نکروزه در طیور استفاده شوند [40].
سپس در مطالعه دیگری، دانشمندان تلاش کردند تا اسپورها را برای رساندن آنتیژن به سیتوپلاسم سلول میزبان مهندسی کنند. این رویکرد میتواند برای تعدادی از اهداف پیشگیرانه و درمانی مانند واکسنهای ضدپاتوژنهای داخل سلولی، واکسیناسیون سلولهای دندریتیک و برای هدف قرار دادن داروهای ضدسرطان مفید باشد. [41].
در سال 2010، مشخص شد فعالیت ادجوانتی اسپورها با اتصال آنتیژن به سطح اسپور ایجاد میشود. اسپورها به عنوان حامل آنتیژن عمل میکنند و شباهت زیادی به خواص ادجوانتهای ریزذرات دارند. این مطالعه یک کاربرد خاص و جدید از اسپورهای باکتریایی را گزارش میکند که در آن آنتیژن میتواند روی سطح اسپور تثبیت شده و از طریق یک مسیر مخاطی وارد بدن شود و طیف وسیعی از پاسخهای ایمنی ایجاد میکند. بدین ترتیب اسپورها بدون نیاز به اصلاح ژنتیکی توانایی عمل به عنوان ادجوانت مخاطی را دارند. این دانشمندان همچنین نشان دادند ترکیبی از فعل و انفعالات الکترواستاتیک و آبگریز مسئول اتصال یک پروتئین به سطح اسپور است [42].
بین سالهای 2010 تا 2020، بسیاری مطالعات دیگر نیز روی اسپور باکتری باسیلوس سوبتیلیس و کاربرد آن در تولید واکسنهای مخاطی برای واکسیناسیون علیه بیماریهای آنفلوآنزا [43]، HIV [44]، عفونت Clonorchis Sinensis [45، 46]، بیماری سل [47]، عفونت سالمونلا [48] و سندروم لکه سفید [49] انجام شد که برخی از از روشهای ژنتیکی و برخی دیگر از روشهای غیرژنتیکی برای اتصال آنتیژن به سطح اسپور استفاده کردهاند.
در مطالعه دیگری در 2020، آنتیژن محافظ که یکی از ۳ عامل بیماریزای اصلی مرتبط با سیاهزخم است روی سطح اسپورهای باسیلوس سوبتیلیس نمایش داده شد. موشها به صورت خوراکی، داخل بینی، زیر زبانی یا داخل صفاقی با واکسن اسپور پروبیوتیک آنتیژن محافظ ایمن شدند. مشاهدات بالینی، تجزیهوتحلیل سرولوژیکی نشان داد موشهای واکسینهشده با واکسن اسپور آنتیژن محافظ از طرق مختلف، سطح تیتر آنتیبادی فعال، پروفایلهای ایزوتیپ و آنتیبادی خنثیکننده سم در سرم و IgA در بزاق را افزایش دادند [14].
در همهگیری اخیر کووید-19 و به دلیل عدم وجود درمانهای دارویی مؤثر، توسعه و استفاده از واکسنهای مؤثر و بیخطر کووید-19 به یک استراتژی مهم برای کنترل شیوع این بیماری تبدیل شده است. در یکی از جدیدترین مطالعات، چانچائو سانگ و همکاران، دمین متصلشونده به گیرنده پروتئین اسپایک (SARS-CoV-19 (sRBD روی سطح اسپور باسیلوس سوبتیلیس نمایش دادند (تصویر شماره 3) و پس از تجویز خوراکی آن به عنوان واکسن، افزایش قابلتوجهی در آنتیبادی خنثیکننده علیه sRBD، هم در موش و هم در انسان مشاهده شد. دمین متصلشونده به گیرنده روی پروتئین اسپایک در پوشش ویروس بیان شده و هدف اصلی برای خنثیسازی توسط آنتیبادیها است. مزیت استفاده از ناقل باسیلوسی نسبت به آدنوویروس این است که باسیلوس سوبتیلیس نسبتاً ایمن است. علاوه بر این، انعقاد خون ایجاد نمیکند، زیرا ناقل باکتری وارد جریان خون نمیشود. واکسنهای سوبتیلیس هزینه تولید کمتری نیز دارند [50].

کاربرد اسپور به عنوان ادجوانت
با افزایش تعداد واکسنهای مبتنی بر پروتئین علیه پاتوژنهای عفونی، توسعه ادجوانتها برای واکسنها به یک حوزه مهم تحقیقاتی تبدیل شده است. مطالعات اخیر نشان داد اسپورهای باسیلوس سوبتیلیس زمانی که همزمان با پروتئینهای آنتیژنی خالصشده تجویز میشوند، ظرفیت ادجوانتی قوی دارند. مطالعات نشان دادهاند زمانی که اسپورهای باسیلوس سوبتیلیس همزمان با یک آنتیژن محلول تجویز شوند، نه تنها ایمنی ذاتی را
تقویت میکنند و در برابر عفونتهای تنفسی محافظت ایجاد میکنند، بلکه باعث افزایش آنتیبادی اختصاصی آنتیژن و تحریک پاسخهای ایمنی سلولی T میشوند. مزیت دیگر اسپورهای باسیلوس سوبتیلیس به عنوان ادجوانت در واکسنهای آنفلوآنزا شامل افزایش اثر واکسن و کاهش دفعات ایمنسازی مورد نیاز برای پاسخ ایمنی بهینه برای محافظت کامل است [51].
در مطالعه سونگ و همکاران، از اسپورهای گرمای کشتهشده باکتری باسیلوس سوبتیلیس به عنوان یک سیستم انتقال واکسن با خواص ادجوانتی مخاطی برای آنفلوآنزا استفاده و خواص آن ارزیابی شد [43].
همچنین در مطالعه دِ آلمیدا و همکاران، به منظور تولید یک واکسن علیه مالاریا از اسپور باسیلوس سوبتیلیس سویه KO7 فیوژ شده با پروتئین CSP نوترکیب پلاسمادیوم فالسی پاروم (rPfCSP) استفاده شد و پاسخ ایمنی هومورال ناشی از ایمیونیزاسیون از طریق مسیر بینی در موش Balb/C ارزیابی شد. نتایج این مطالعه نشان داد اسپورهای همراه با rPfCSP ایمنیزایی آنتیژن را افزایش میدهند و سطوح بالایی از IgG سرمی را القا میکنند. دادههای این مطالعه نشان داد استفاده از اسپور به عنوان ادجوانت میتواند پاسخ آنتیبادی بیشتر، سریعتر و طولانیتر را علیه آنتیژن PfCSP تحریک کند. علاوه بر این، نشان داده شد این رویکرد واکسن بسیار امیدوارکننده است، زیرا ممکن است پاسخ ایمنی متعادل Th1/Th2 را القا کند [52].
میزان ایمنیزایی واکسنهای مخاطی بر پایه اسپور
واکسیناسیون مخاطی از طریق تجویز خوراکی یا داخل بینی میتواند پاسخهای ایمنی مؤثری را در برابر عفونتهای مرتبط با موانع مخاطی مانند دستگاه گوارش (GIT=Gastrointestinal tract)، دستگاه تناسلی و حفره دهان ایجاد کند. اسپورهای باسیلوس سوبتیلیس برای ایمنسازی مخاطی به دلیل چندین ویژگی جذاب که شامل سابقه ایمنی استفاده از آنها در انسان و حیوان، مقاومت به pH اسیدی (برای تجویز خوراکی) و سهولت دستکاری ژنتیکی است، بررسی شده است. نکته مهم این است که اسپورهای باسیلوس سوبتیلیس میتوانند با سلولهای ایمنی تعامل داشته باشند و هنگام عبور از دستگاه گوارش باعث تولید پاسخ ایمنی محافظتی سیستم ایمنی بدن شوند [13].
مشخص شد اسپورهای باسیلوس سوبتیلیس ابزار ارزشمندی برای تحریک پاسخهای ایمنی قویتر با افزایش نمایش آنتیژن هستند [53]. علاوه بر پاسخهای ایمنی به واسطه آنتیبادی، مطالعات بیشتر نشان داد اسپورهای نوترکیب پاسخ سلولی سلولهایT CD4+/CD8+ اختصاصی آنتیژن را تقویت میکنند. مطالعات دیگر نشان دادهاند اسپور باسیلوس سوبتیلیس توسط TLR2 ،TLR4 و TLR9 نیز شناخته میشود و میتواند پاسخهای Th1/Th2 را با حضور IgG2a و IgG1 در سرم موشهای ایمنشده القا کند [43].
مقایسه ایمنیزایی واکسنهای مخاطی بر پایه اسپور با سایر واکسنها
واکسنهای دارای مجوز در حال حاضر از طریق یکی از ۵ مسیر اصلی تجویز میشوند که تجویز عضلانی، رایجترین آن است و چندین واکسن مانند هپاتیت A و B، هاری، آنفلوآنزا، دیفتری، کزاز و سیاه سرفه با این روش تزریق میشود. مسیرهای زیرجلدی و داخل پوستی نیز رایج است و به ترتیب برای واکسیناسیون سرخک، اوریون، سرخجه، تب زرد و (واکسن ضدبیماری سل)- هاری استفاده میشود. ۲ مسیر باقیمانده آنتیژنها را به سطوح مخاطی بینی یا روده میرساند. از راه داخل بینی، برای مثال، برای ویروسهای آنفلوآنزای ضعیفشده زنده استفاده میشود، در حالی که مسیر دهانی برای واکسیناسیون فلج اطفال، وبا، روتاویروس و تب حصبه استفاده میشود [54].
مزایای زیادی وجود دارد که واکسنهای مخاطی را جایگزین جذابی برای واکسنهایی میکند که از راههای سیستمیک تجویز میشوند. ازجمله اینکه پاسخهای ایمنی محافظتی را میتوان در درگاههای مخاطی مربوط به ورود پاتوژن با تحویل واکسنها به مخاط القا کرد. نمونههای متعددی به وضوح اعتبار این استراتژی را نشان میدهد، ازجمله واکسنهای ویروس آنفلوآنزای غیرفعال یا ضعیفشده داخل بینی، واکسن فلج اطفال خوراکی و واکسنهای تضعیفشده خوراکی سالمونلا تیفی و ویبریو کلرا و بسیاری دیگر که در حال حاضر در حال توسعه علیه عفونتهای مختلف رودهای و تنفسی هستند [55].
همچنین نتایج حاصل از چندین مطالعه اخیر اهمیت پاسخهای ایمنی مخاطی در برابر SARS-CoV-2 را برجسته میکند. این مطالعات نشان میدهد که تجویز داخل بینی به عنوان یک استراتژی جذابتر برای تحریک پاسخ های ایمنی محافظتی اولیه در مخاط دستگاه تنفسی فوقانی قبل از اینکه SARS-CoV-2 جای پایی در دستگاه تنفسی تحتانی پیدا کند، است [56].
علاوه بر این، در اپیدمیهای ناشی از عفونتهای منتقله از طریق مخاط، ایمنسازی انبوه از راههای مخاطی احتمالاً عملیتر و کمهزینهتر از ایمنسازی از راههای سیستمیک است. همچنین کاهش هزینه واکسنهای مخاطی در هر ۲ سطح تولید و تحویل محقق میشود. خلوص واکسنهای تحویل دادهشده از طریق مخاط، ازجمله آلودگی به اندوتوکسین، نسبت به واکسنهای تزریقی اهمیت کمتری دارد. برخی از واکسنهای مخاطی نیازی به نگهداری در دمای پایین ندارند و زمانی که در دمای محیط برای مدت طولانی نگهداری شوند، پایدار و کاملاً ایمونوژن باقی میمانند. درنهایت، تحویل واکسن مخاطی به سرنگها و سوزنهای استریل یا پرسنل آموزشدیده برای استفاده و دفع آنها نیاز ندارد، اگرچه ممکن است دستگاههای اسپری یا سایر اعمالکنندهها برای تزریق داخل بینی و سایر راههای تزریق مورد نیاز باشد [55].
بحث
مطالعه حاضر نشان داد واکسنهای مخاطی مبتنی بر اسپور مزایای بیشماری مانند کمک به واکسیناسیون انبوه با افزایش سهولت و سرعت تحویل، کاهش هزینهها با حذف مراحل تصفیه و تجویز منعطف از طریق مسیرهای مخاطی یا دهانی و سیستمهای تحویل واکسن بدون سوزن و بدون یخچال را ارائه میدهند [57].
یکی دیگر از ویژگیهای منحصربهفرد واکسنهای مخاطی مبتنی بر اسپور این است که اسپورها نانوساختارهایی در مقیاس زیر میکرون دارند که به آنها اجازه میدهد تا به عنوان ادجوانتهای ذرهای مؤثر عمل کنند. ادجوانتهای ذرهای به طور مؤثر سلولهای ارائهدهنده آنتیژن را هدف قرار میدهند و پس از درونی شدن در سلول، توسط مجموعه سازگاری بافتی اصلی کلاس I و کلاس II پردازش میشوند که منجر به ارائه آنتیژن در سطح APC میشود.
همچنین مطالعاتی که خاصیت ادجوانتی اسپورهای باسیلوس سوبتیلیس را بررسی میکنند، نشان میدهند که اثرات ادجوانتی قوی زمانی مشاهده میشوند که اسپورها با آنتیژنهای پروتئینی که مخلوط یا جذبشده روی سطح پوشش اسپور هستند، تجویز میشوند. به علاوه، مشخص شده که اندازه ذرات اسپور برای تقویت ایمنی مخاطی مناسب است؛ بنابراین انعطافپذیری اسپورها، همراه با یک مسیر مخاطی تحویل، واکسنهای اسپور را به کاندیدایی امیدوارکننده تبدیل میکند، به ویژه زمانی که تولید انبوه و واکسیناسیون در مقیاس بزرگ به فوریت مورد نیاز باشد [58].
محدودیتهای واکسنهای مخاطی بر پایه اسپور باسیلوس سوبتیلیس
با وجود تمام مزایای واکسنهای مخاطی مبتنی بر اسپور، استفاده از این نوع واکسنها معایبی نیز دارد؛ بنابراین در استفاده از آنها باید به نکات ایمنی و اخلاقی توجه کرد. چنانچه اسپورها به طور کامل غیرفعال نشده باشند و در شرایط بهینه رشد قرار گیرند، به فرم فعال باکتریایی تبدیل میشوند؛ بنابراین باید مشخص باشد که چه نسبتی از اسپورها ممکن است جوانه بزنند و آیا این امر قابل کنترل است یا نه؟ همچنین واکسنهای مخاطی باید بر مشکلات مرتبط با جذب ضعیف یا تخریب در سیستم گوارش غلبه کنند [54].
مشکل دیگر استفاده از اسپورها به عنوان ناقل واکسن در مورد واکسنهای حیوانی است. اسپورهای نوترکیبی که به عنوان واکسن در حیوانات استفاده میشوند، میتوانند از طریق مدفوع، وارد محیط زیست شوند و این امر موجب تجمع اسپورهای نوترکیب در محیط میشود. از سوی دیگر، اگرچه باکتری باسیلوس سوبتیلیس به عنوان یک باکتری ایمن شناخته میشود، اما ممکن است گاهی با عفونتهای فرصت طلب مرتبط باشد؛ بنابراین باید از گونههای باکتری کاملاً شناخته شده استفاده کرد.
نتیجهگیری
به طور کلی اسپورها مقاومت خوبی در برابر استرس دارند؛ بنابراین واکسنهایی که با این روش تولید میشوند، میتوانند محیط اسیدی دستگاه گوارش را تحمل کنند و ماندگاری طولانیمدت داشته باشند. آنها میتوانند به آرامی از مخاط دستگاه گوارش عبور کنند و به سرعت سیستم ایمنی بدن را وادار به تولید یک پاسخ ایمنی محافظتی کنند. علاوه بر این، استفاده از اسپور به عنوان حامل واکسن میتواند کارایی پاسخ ایمنی را بهبود ببخشد.
واکسنهای خوراکی باسیلوس سوبتیلیس سهم قابلتوجهی در پیشگیری و درمان کووید-۱۹ در آینده خواهند داشت. هر چند در حال حاضر، هیچ واکسن در دسترس تجاری از یک ناقل باسیلوسی وجود ندارد. اسپورهای باسیلوس سوبتیلیس به عنوان ناقل واکسنها میتوانند کمک قابل توجهی در پیشگیری و درمان بیماریها در آینده داشته باشند.
در پژوهش حاضر سعی شد از تمام منابع مرتبط با موضوع استفاده شود، اما زیاد بودن تعداد منابع و احتمال از دست دادن برخی از آنها و نیز عدم دسترسی به متن کامل برخی از مقالات، ازجمله محدودیتهای این مطالعه است. همچنین باکتری باسیلوس سوبتیلیس و اسپور آن کاربردهای بسیاری دارد که در این پژوهش تنها به قسمتی از آن اشاره شده است.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
همه اصول اخلاقی در نگارش این مقاله، طبق دستورالعمل کمیته ملی اخلاق و آییننامه COPE رعایت شده است.
حامی مالی
این پژوهش هیچگونه کمک مالی از سازمانهای دولتی، خصوصی و غیرانتفاعی دریافت نکرده است.
مشارکت نویسندگان
طرح ایده اولیه: غلامرضا احمدیان؛ مطالعه، پژوهش و نگارش مقاله: سمیرا قائدمحمدی، حورا بحرالعلوم؛ بازبینی: غلامرضا احمدیان، سمیرا قائدمحمدی.
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
References
- Isticato R, Cangiano G, Tran HT, Ciabattini A, Medaglini D, Oggioni MR, et al. Surface display of recombinant proteins on Bacillus subtilis spores. J Bacteriol. 2001; 183(21):6294-301. [DOI:10.1128/JB.183.21.6294-6301.2001] [PMID] [PMCID]
- Iwanicki A, Piatek I, Stasiłojć M, Grela A, Łega T, Obuchowski M, et al. A system of vectors for Bacillus subtilis spore surface display. Microb Cell Fact. 2014; 13(1):30. [DOI:10.1186/1475-2859-13-30] [PMID] [PMCID]
- Charbit A, Boulain JC, Ryter A, Hofnung M. Probing the topology of a bacterial membrane protein by genetic insertion of a foreign epitope; expression at the cell surface. EMBO J. 1986; 5(11):3029-37. [PMID]
- Freudl R, MacIntyre S, Degen M, Henning U. Cell surface exposure of the outer membrane protein OmpA of Escherichia coli K-12. J Mol Biol. 1986; 188(3):491-4. [DOI:10.1016/0022-2836(86)90171-3] [PMID]
- Fasehee H, Rostami A, Ramezani F, Ahmadian G. Engineering E. Coli cell surface in order to develop a one-step purification method for recombinant proteins. AMB Express. 2018; 8(1). [DOI:10.1186/s13568-018-0638-8] [PMID] [PMCID]
- Vahed M, Ramezani F, Tafakori V, Mirbagheri VS, Najafi A, Ahmadian G. Molecular dynamics simulation and experimental study of the surface-display of SPA protein via Lpp-OmpA system for screening of IgG. AMB Express. 2020; 10(1):161. [DOI:10.1186/s13568-020-01097-1] [PMID] [PMCID]
- Tafakori V, Ahmadian G, Amoozegar MA. Surface display of bacterial metallothioneins and a chitin binding domain on escherichia coli increase cadmium adsorption and cell immobilization. Appl Biochem Biotechnol. 2012; 167(3):462-73. [DOI:10.1007/s12010-012-9684-x] [PMID]
- Smith GP. Filamentous fusion phage: Novel expression vectors that display cloned antigens on the virion surface. Science. 1985; 228(4705):1315-7. [DOI:10.1126/science.4001944] [PMID]
- Lee SY, Choi JH, Xu Z. Microbial cell-surface display. Trends Biotechnol. 2003; 21(1):45-52. [DOI:10.1016/S0167-7799(02)00006-9] [PMID]
- Boder ET, Wittrup KD. Yeast surface display for screening combinatorial polypeptide libraries. Nat Biotechnol. 1997; 15(6):553-7. [DOI:10.1038/nbt0697-553] [PMID]
- Guoyan Z, Yingfeng A, Zabed H, Qi G, Yang M, Jiao Y, et al. Bacillus subtilis spore surface display technology: A review of its development and applications. J Microbiol Biotechnol. 2019; 29(2):179-90. [DOI:10.4014/jmb.1807.06066] [PMID]
- Lin P, Yuan H, Du J, Liu K, Liu H, Wang T. Progress in research and application development of surface display technology using Bacillus subtilis spores. Appl Microbiol Biotechnol. 2020; 104(6):2319-31. [DOI:10.1007/s00253-020-10348-x] [PMID] [PMCID]
- Zhang X, Al-Dossary A, Hussain M, Setlow P, Li J. Applications of bacillus subtilis spores in biotechnology and advanced materials. Appl Environ Microbiol. 2020; 86(17):e01096-20. [DOI:10.1128/AEM.01096-20.] [PMID] [PMCID]
- Oh Y, Kim JA, Kim CH, Choi SK, Pan JG. Bacillus subtilis spore vaccines displaying protective antigen induce functional antibodies and protective potency. BMC Vet Res. 2020; 16(1):259. [DOI:10.1186/s12917-020-02468-3] [PMID] [PMCID]
- Ferreira LC, Ferreira RC, Schumann W. Bacillus subtilis as a tool for vaccine development: From antigen factories to delivery vectors. An Acad Bras Cienc. 2005; 77(1):113-24. [DOI:10.1590/S0001-37652005000100009] [PMID]
- Hinc K, Ghandili S, Karbalaee G, Shali A, Noghabi KA, Ricca E, et al. Efficient binding of nickel ions to recombinant Bacillus subtilis spores. Res Microbiol. 2010; 161(9):757-64.[DOI:10.1016/j.resmic.2010.07.008] [PMID]
- Ahmadian G, Keshavarz M, Ahmadi Zeydabadi M. [Cloning and expression of Recombinant antifungal chitinase enzyme of Bacillus pumilus in Bacillus subtilis 168 (Persian)]. Koomesh. 2012; 13(2):151-8. [Link]
- Rostami A, Hinc K, Goshadrou F, Shali A, Bayat M, Hassanzadeh M, et al. Display of B. pumilus chitinase on the surface of B. subtilis spore as a potential biopesticide. Pestic Biochem Physiol. 2017; 140:17-23. [DOI:10.1016/j.pestbp.2017.05.008] [PMID]
- Ghaedmohammadi S, Ahmadian G. The first report on the sortase-mediated display of bioactive protein A from Staphylococcus aureus (SpA) on the surface of the vegetative form of Bacillus subtilis. Microb Cell Fact. 2021; 20(1):212. [DOI:10.1186/s12934-021-01701-4] [PMID] [PMCID]
- Tan IS, Ramamurthi KS. Spore formation in Bacillus subtilis. Environ Microbiol Rep. 2013; 6(3):212-25. [DOI:10.1111/1758-2229.12130] [PMID] [PMCID]
- Fujita M, Losick R. Evidence that entry into sporulation in Bacillus subtilis is mediated by gradual activation of a master regulator spo0A. Genes Dev. 2005; 19(18):2236-44. [DOI:10.1101/gad.1335705] [PMID] [PMCID]
- McKenney PT, Driks A, Eichenberger P. The Bacillus subtilis endospore: Assembly and functions of the multilayered coat. Nat Rev Microbiol. 2013; 11(1):33-44. [DOI:10.1038/nrmicro2921] [PMID] [PMCID]
- Cowan AE, Koppel DE, Setlow B, Setlow P. A soluble protein is immobile in dormant spores of Bacillus subtilis but is mobile in germinated spores: Implications for spore dormancy. Proc Natl Acad Sci U S A. 2003; 100(7):4209-14. [DOI:10.1073/pnas.0636762100] [PMID] [PMCID]
- McKenney PT, Eichenberger P. Dynamics of spore coat morphogenesis in Bacillus subtilis. Mol Microbiol. 2012; 83(2):245-60. [DOI:10.1111/j.1365-2958.2011.07936.x] [PMID] [PMCID]
- Isticato R, Cangiano G, Tran HT, Ciabattini A, Medaglini D, Oggioni MR, et al. Surface display of recombinant proteins on Bacillus subtilis spores. J Bacteriol. 2001; 183(21):6294-301. [DOI:10.1128/JB.183.21.6294-6301.2001] [PMID] [PMCID]
- Isticato R, Di Mase DS, Mauriello EMF, De Felice M, Ricca E. Amino terminal fusion of heterologous proteins to CotC increases display efficiencies in the Bacillus subtilis spore system. Biotechniques. 2007; 42(2):151-2, 154, 156. [DOI:10.2144/000112329] [PMID]
- Hinc K, Isticato R, Dembek M, Karczewska J, Iwanicki A, Peszyńska-Sularz G, et al. Expression and display of UreA of Helicobacter acinonychis on the surface of Bacillus subtilis spores. Microb Cell Fact. 2010; 9:2. [DOI:10.1186/1475-2859-9-2] [PMID] [PMCID]
- Potot S, Serra CR, Henriques AO, Schyns G. Display of recombinant proteins on Bacillus subtilis spores, using a coat-associated enzyme as the carrier. Appl Environ Microbiol. 2010; 76(17):5926-33. [DOI:10.1128/AEM.01103-10] [PMID] [PMCID]
- Naclerio G, Baccigalupi L, Zilhao R, De Felice M, Ricca E. Bacillus subtilis spore coat assembly requires cotH gene expression. J Bacteriol. 1996; 178(15):4375-80. [DOI:10.1128/jb.178.15.4375-4380.1996] [PMID] [PMCID]
- Hinc K, Iwanicki A, Obuchowski M. New stable anchor protein and peptide linker suitable for successful spore surface display in B. subtilis. Microb Cell Fact. 2013; 12:22. [DOI:10.1186/1475-2859-12-22] [PMID] [PMCID]
- Sirec T, Strazzulli A, Isticato R, De Felice M, Moracci M, Ricca E. Adsorption of β-galactosidase of Alicyclobacillus acidocaldarius on wild type and mutants spores of Bacillus subtilis. Microb Cell Fact. 2012; 11:100. [DOI:10.1186/1475-2859-11-100] [PMID] [PMCID]
- Yim SK, Jung HC, Yun CH, Pan JG. Functional expression in Bacillus subtilis of mammalian NADPH-cytochrome P450 oxidoreductase and its spore-display. Protein Expr Purif. 2009; 63(1):5-11. [DOI:10.1016/j.pep.2008.07.004] [PMID]
- Gashtasbi F, Ahmadian G, Noghabi KA. New insights into the effectiveness of alpha-amylase enzyme presentation on the Bacillus subtilis spore surface by adsorption and covalent immobilization. Enzyme Microb Technol. 2014; 64-65:17-23. [DOI:10.1016/j.enzmictec.2014.05.006] [PMID]
- Ghaedmohammadi S, Rigi G, Zadmard R, Ricca E, Ahmadian G. Immobilization of Bioactive Protein A from Staphylococcus aureus (SpA) on the Surface of Bacillus subtilis Spores. Mol Biotechnol. 2015; 57(8):756-66. [DOI:10.1007/s12033-015-9868-z] [PMID]
- Duc le H, Hong HA, Fairweather N, Ricca E, Cutting SM. Bacterial spores as vaccine vehicles. Infect Immun. 2003; 71(5):2810-8. [DOI:10.1128/IAI.71.5.2810-2818.2003] [PMID] [PMCID]
- Ricca E, Baccigalupi L, Cangiano G, De Felice M, Isticato R. Mucosal vaccine delivery by non-recombinant spores of Bacillus subtilis. Microbial Cell Factories. 2014; 13:115. [PMID]
- Medaglini D, Ricci S, Maggi T, Rush CM, Manganelli R, Oggioni MR, et al. Recombinant Gram-positive bacteria as vehicles of vaccine antigens. Biotechnol Annu Rev. 1997; 3(C):297-312. [DOI:10.1016/S1387-2656(08)70038-3]
- Duc le H, Hong HA, Atkins HS, Flick-Smith HC, Durrani Z, Rijpkema S, et al. Immunization against anthrax using Bacillus subtilis spores expressing the anthrax protective antigen. Vaccine. 2007; 25(2):346-55. [DOI:10.1016/j.vaccine.2006.07.037] [PMID]
- Barnes AG, Cerovic V, Hobson PS, Klavinskis LS. Bacillus subtilis spores: A novel microparticle adjuvant which can instruct a balanced Th1 and Th2 immune response to specific antigen. Eur J Immunol. 2007; 37(6):1538-47. [DOI:10.1002/eji.200636875] [PMID]
- Hoang TH, Hong HA, Clark GC, Titball RW, Cutting SM. Recombinant Bacillus subtilis expressing the Clostridium perfringens alpha toxoid is a candidate orally delivered vaccine against necrotic enteritis. Infect Immun. 2008; 76(11):5257-65. [DOI:10.1128/IAI.00686-08] [PMID] [PMCID]
- Huang JM, La Ragione RM, Cooley WA, Todryk S, Cutting SM. Cytoplasmic delivery of antigens, by Bacillus subtilis enhances Th1 responses. Vaccine. 2008; 26(48):6043-52. [DOI:10.1016/j.vaccine.2008.09.024] [PMID]
- Huang JM, Hong HA, Van Tong H, Hoang TH, Brisson A, Cutting SM. Mucosal delivery of antigens using adsorption to bacterial spores. Vaccine. 2010; 28(4):1021-30. [DOI:10.1016/j.vaccine.2009.10.127] [PMID]
- Song M, Hong HA, Huang JM, Colenutt C, Khang DD, Nguyen TV, et al. Killed Bacillus subtilis spores as a mucosal adjuvant for an H5N1 vaccine. Vaccine. 2012; 30(22):3266-77. [DOI:10.1016/j.vaccine.2012.03.016] [PMID]
- de Souza RD, Batista MT, Luiz WB, Cavalcante RC, Amorim JH, Bizerra RS, et al. Bacillus subtilis spores as vaccine adjuvants: Further insights into the mechanisms of action. PLoS One. 2014; 9(1):e87454. [DOI:10.1371/journal.pone.0087454] [PMID] [PMCID]
- Sun H, Lin Z, Zhao L, Chen T, Shang M, Jiang H, et al. Bacillus subtilis spore with surface display of paramyosin from Clonorchis sinensis potentializes a promising oral vaccine candidate. Parasit Vectors. 2018; 11(1):156. [DOI:10.1186/s13071-018-2757-0] [PMID] [PMCID]
- Zhou Z, Xia H, Hu X, Huang Y, Li Y, Li L, et al. Oral administration of a Bacillus subtilis spore-based vaccine expressing Clonorchis sinensis tegumental protein 22.3 kDa confers protection against Clonorchis sinensis. Vaccine. 2008; 26(15):1817-25. [DOI:10.1016/j.vaccine.2008.02.015] [PMID]
- Sibley L, Reljic R, Radford DS, Huang JM, Hong HA, Cranenburgh RM, et al. Recombinant Bacillus subtilis spores expressing MPT64 evaluated as a vaccine against tuberculosis in the murine model. FEMS Microbiol Lett. 2014; 358(2):170-9. [DOI:10.1111/1574-6968.12525] [PMID]
- Dai X, Liu M, Pan K, Yang J. Surface display of OmpC of Salmonella serovar Pullorum on Bacillus subtilis spores. PLoS One. 2018; 13(1):e0191627. [DOI:10.1371/journal.pone.0191627] [PMID] [PMCID]
- Nguyen AT, Pham CK, Pham HT, Pham HL, Nguyen AH, Dang LT, et al. Bacillus subtilis spores expressing the VP28 antigen: A potential oral treatment to protect Litopenaeus vannamei against white spot syndrome. FEMS Microbiol Lett. 2014; 358(2):202-8. [DOI:10.1111/1574-6968.12546] [PMID]
- CSung JC, Liu Y, Wu KC, Choi MC, Ma CH, Lin J, et al. Expression of SARS-CoV-2 Spike Protein Receptor Binding Domain on Recombinant B. subtilis on Spore Surface: A Potential Expression of SARS-CoV-2 Spike Protein Receptor Binding Domain on Recombinant B. subtilis on Spore Surface: A Potential COVID-19 Oral Vaccine Candidate. Vaccines (Basel). 2021; 10(1):2. [PMID] [PMCID]
- Lee JE, Kye YC, Park SM, Shim BS, Yoo S, Hwang E, et al. Bacillus subtilis spores as adjuvants against avian influenza H9N2 induce antigen-specific antibody and T cell responses in White Leghorn chickens. Vet Res. 2020; 51(1):68. [PMID] [PMCID]
- de Almeida ME, Alves KC, de Vasconcelos MG, Pinto TS, Glória JC, Chaves YO, et al. Bacillus subtilis spores as delivery system for nasal Plasmodium falciparum circumsporozoite surface protein immunization in a murine model. Sci Rep. 2022;12(1):1531. [Link]
- Mauriello EM, Cangiano G, Maurano F, Saggese V, De Felice M, Rossi M, et al. Germination-independent induction of cellular immune response by Bacillus subtilis spores displaying the C fragment of the tetanus toxin. Vaccine. 2007; 25(5):788-93. [DOI:10.1016/j.vaccine.2006.09.013] [PMID]
- Cutting SM, Hong HA, Baccigalupi L, Ricca E. Oral vaccine delivery by recombinant spore probiotics. Int Rev Immunol. 2009; 28(6):487-505. [PMID]
- Mestecky J, Lamm ME, Ogra PL, Strober W, Bienenstock J, McGhee JR, et al. Mucosal immunology. Amsterdam: Elsevier; 2005. [Link]
- Kyriakidis NC, López-Cortés A, González EV, Grimaldos AB, Prado EO. SARS-CoV-2 vaccines strategies: A comprehensive review of phase 3 candidates. NPJ Vaccines. 2021; 6(1):28. [PMID]
- Pan JG, Kim EJ, Yun CH. Bacillus spore display. Trends Biotechnol. 2012; 30(12):610-2. [DOI:10.1016/j.tibtech.2012.09.005] [PMID]
- Oh Y. Potential for mucosal delivery of bacillus subtilis spore vaccines displaying immunogenic protein on the surface. Arch Clin Microbiol .2021; 12(s2):1-4.[Link]
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |








